Активни састојци: Прасугрел
Ефиент 10 мг филмом обложене таблете
Ефиент 5 мг филм таблете
Зашто се користи Ефиент? За шта је то?
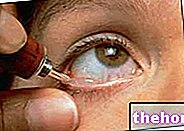
Ефиент, који садржи активну супстанцу прасугрел, припада групи лекова који се зову тромбоцитни агенси. Тромбоцити су врло мале ћелије које циркулишу у крви. Када је крвни суд оштећен, на пример ако је пререзан, тромбоцити се згрушавају заједно како би допринели стварању крвног угрушка (тромба). Стога су тромбоцити неопходни за заустављање крварења. Ако се угрушци формирају у отврднутом крвном суду, попут артерије, могу бити врло опасни јер могу блокирати пролаз крви, узрокујући срчани удар (инфаркт миокарда), мождани удар или смрт Угрушци у артеријама који носе крв до срца такође могу смањити проток крви у срце, узрокујући нестабилну ангину (тешки бол у грудима).
Ефиент инхибира агрегацију тромбоцита и стога смањује могућност стварања крвних угрушака.
Ефиент вам је прописан јер сте претходно имали срчани удар или нестабилну ангину и лечили сте се процедуром за отварање блокираних срчаних артерија. Можда сте такође ставили један или више стентова у блокирану или сужену артерију како бисте обновили проток крви. Ефиент смањује шансе да доживите још један срчани удар или мождани удар или умрете од неког од ових атеротромботичних догађаја. Ваш лекар ће вам такође прописати ацетилсалицилну киселину ( тј. аспирин), још један лек против тромбоцита.
Контраиндикације Када се Ефиент не сме користити
Немојте узимати Ефиент
- Ако сте алергични (преосетљиви) на прасугрел или неки други састојак лека Ефиент. Алергијска реакција се може препознати јер изазива осип, свраб, отицање лица, отицање усана или пискање. Ако се појави било шта од наведеног, одмах обавестите свог лекара.
- Ако имате здравствено стање које узрокује крварење, попут крварења у желуцу или цревима.
- Ако сте раније имали мождани удар или пролазни исхемијски напад (ТИА).
- Ако имате тешку болест јетре.
Предострожности при употреби Шта треба да знате пре него што узмете лек Ефиент
Ако се догоди било која од доле наведених ситуација, реците свом лекару пре него што узмете Ефиент:
- Ако имате повећан ризик од крварења, као што су:
- 75 година или више. Ваш лекар ће прописати дневну дозу од 5 мг јер постоји повећан ризик од крварења код пацијената старијих од 75 година.
- недавна тешка траума
- недавна операција (укључујући неке стоматолошке захвате)
- недавно или понављајуће крварење у желуцу или цревима (на пример чир на желуцу или полип дебелог црева)
- телесна тежина мања од 60 кг. Ваш лекар ће вам прописати дневну дозу од 5 мг Ефиента ако је ваша тежина мања од 60 кг - умерено обољење јетре или бубрега
- ако узимате одређене лекове (погледајте "Узимање лека Ефиент са другим лековима")
- ако имате заказану операцију (укључујући неке стоматолошке захвате) у наредних седам дана. Ваш лекар вам може саветовати да привремено престанете са узимањем лека Ефиент због повећаног ризика од крварења
- Ако сте икада имали алергијске реакције (преосетљивости) на клопидогрел или било који други лек против тромбоцита, обавестите свог лекара пре почетка лечења Ефиентом.Ако тада узмете лек Ефиент и доживите алергијске реакције које се могу препознати као „осип, свраб, отицање лица, отечене усне или отежано дисање, одмах обавестите свог лекара.
Док узимате Ефиент:
Одмах обавестите свог лекара ако развијете здравствено стање под називом тромботична тромбоцитопенична пурпура (ПТТ), које укључује грозницу и модрице испод коже које се могу појавити као ситне црвене тачкице, са или без необјашњивог дубоког умора, збуњености, промене боје. Жута кожа или очи (жутица) (видети одељак 4 "Могући нежељени ефекти").
Деца и адолесценти
Ефиент није за употребу код деце и адолесцената млађих од 18 година.
Интеракције Који лекови или храна могу променити ефекат Ефиента
Обавестите свог лекара ако узимате, недавно сте узимали или бисте могли узети било које друге лекове, укључујући лекове који се издају без рецепта, дијететске суплементе и биљне лекове. Посебно је важно да свом лекару кажете ако се лечите клопидогрелом (леком против тромбоцита), варфарином (антикоагулансом) или „нестероидним антиинфламаторним лековима“ за ублажавање болова и смањење температуре (попут ибупрофена, напроксен, еторикоксиб). Када се дају у комбинацији са Ефиентом, ови лекови могу повећати ризик од крварења.
Узимајте друге лекове док сте на леку Ефиент само ако вам је лекар рекао да можете.
Упозорења Важно је знати да:
Трудноћа и дојење
Реците свом лекару ако сте трудни или планирате трудноћу док узимате Ефиент. Ефиент бисте требали користити тек након што са лекаром разговарате о могућим користима и потенцијалним ризицима за ваше нерођено дете.
Ако дојите, питајте лекара или фармацеута за савет пре него што узмете било који лек
Вожња и управљање машинама
Није вероватно да ће Ефиент утицати на способност управљања возилима и рада на машинама.
Ефиент садржи лактозу.
Ако вам је лекар рекао да немате интолеранцију на неке шећере, консултујте се са лекаром пре узимања овог лека.
Доза, начин и време примене Како се користи Ефиент: Дозирање
Увек узимајте Ефиент тачно онако како вам је рекао лекар. Ако сте у недоумици, обратите се свом лекару или фармацеуту.
Уобичајена доза Ефиента је 10 мг дневно. Лечење почиње једном дозом од 60 мг. Ако је ваша телесна тежина мања од 60 кг или сте старији од 75 година, доза је 5 мг Ефиента дневно.
Ваш лекар ће вам такође рећи да узимате ацетилсалицилну киселину - он ће вам рећи тачну дозу коју треба да узмете (обично између 75 мг и 325 мг дневно).
Можете узети Ефиент са или без хране. Узимајте Ефиент сваки дан у исто време. Немојте ломити или ломити таблету.
Важно је да свом лекару, фармацеуту и стоматологу кажете да узимате Ефиент.
Предозирање Шта треба учинити ако сте узели превише лека Ефиент
Ако узмете више лека Ефиент него што је требало
Одмах се обратите свом лекару или најближој болници због ризика од прекомерног крварења. Покажите свом лекару своје паковање Ефиента.
Ако сте заборавили да узмете Ефиент
Ако сте заборавили да узмете дозу, узмите једну таблету чим то приметите. Ако сте заборавили да узмете дозу цео дан, само узмите своју нормалну дозу лека Ефиент следећег дана. Не узимајте две дозе истог дана. За паковања од 14, 28, 56, 84 и 98 таблета, можете проверити дан када сте узели последњу таблету Ефиент тако што ћете проверити календар одштампан на блистеру.
Ако престанете да узимате Ефиент
Немојте престати са узимањем лека Ефиент без разговора са лекаром. Ако прерано престанете са узимањем лека Ефиент, ризик од инфаркта миокарда може бити већи.
Ако имате додатних питања о употреби овог лека, обратите се свом лекару или фармацеуту.
Нежељени ефекти Који су нежељени ефекти лека Ефиент
Као и сви лекови, Ефиент може изазвати нежељена дејства, мада се она не морају јавити код свих.
Одмах се обратите лекару ако приметите неки од следећих нежељених ефеката:
- Изненадна поспаност или слабост у руци, нози или лицу, посебно ако је ограничена на једну страну тела
- Изненадна конфузија, потешкоће у говору или разумевању онога што други говоре
- Изненадне потешкоће при ходању или губитак равнотеже или координације
- Изненадна вртоглавица или изненадна јака главобоља без познатог узрока.
Све горе наведено може бити знак можданог удара. Мождани удар је неуобичајен нежељени ефекат лека Ефиент код пацијената који никада нису имали мождани удар или пролазни исхемијски напад (ТИА).
Такође одмах контактирајте свог лекара ако приметите неки од следећих нежељених ефеката:
- грозница и модрице испод коже које се могу појавити као ситне црвене тачкице, са или без необјашњивог дубоког умора, збуњености, жутања коже или очију (жутица) (погледајте одељак 2 "ПРЕ него што почнете да радите")
- "осип на кожи, свраб или отицање лица, отицање усана / језика или пискање. Све ово могу бити знаци озбиљне алергијске реакције (погледајте одељак 2" Шта треба да знате пре него што узмете лек Ефиент “)
Одмах се обратите лекару ако приметите неки од следећих нежељених ефеката:
- Крв у урину
- Крварење из ректума, крв у столици или столица црне боје
- Неконтролисано крварење, на пример од посекотине
Све горе наведено може бити знак крварења, најчешће нуспојаве уз Ефиент. Иако неуобичајено, тешко крварење може бити опасно по живот.
Чести нежељени ефекти (могу се јавити у до 1 на 10 особа)
- Крварење у желуцу или цревима
- Крварење са места убода игле
- Крварење из носа
- Осип по кожи
- Мале црвене модрице на кожи (модрице)
- Крв у урину
- Хематом (крварење испод коже на месту ињекције или у мишић, изазивајући отицање)
- Низак хемоглобин или низак број црвених крвних зрнаца (анемија)
- Модрице
Мање чести нежељени ефекти (могу се јавити у до 1 на 100 људи)
- Алергијска реакција (осип, свраб, отицање усана / језика или пискање)
- Спонтано крварење из ока, ректума, десни или абдомена око унутрашњих органа
- Крварење након операције
- Искашљава крв
- Крв у столици
Ретки нежељени ефекти (могу се јавити у до 1 на 1.000 људи)
- Мали број тромбоцита у крви
- Поткожни хематом (крварење испод коже изазива отицање)
Пријављивање нежељених ефеката
Ако било који од нежељених ефеката постане озбиљан, или ако приметите било који нежељени ефекат који није наведен у овом упутству, обавестите свог лекара или фармацеута. Такође можете пријавити нежељене ефекте директно преко националног система пријављивања наведених у Додатку В.Пријављивањем нежељених ефеката можете помоћи у пружању више информација о безбедности овог лека.
Истек и задржавање
Чувајте Ефиент ван погледа и дохвата деце.
Немојте користити Ефиент након истека рока ваљаности наведеног на блистеру и кутији иза „Рок ваљаности“. Датум истека се односи на последњи дан у месецу.
Чувати у оригиналном паковању ради заштите од ваздуха и влаге.
Лекове не треба одлагати у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Шта садржи Ефиент
- Активни састојак је прасугрел.
Ефиент 10 мг: Свака таблета садржи 10 мг прасугрела (у облику хидрохлорида).
Ефиент 5 мг: Свака таблета садржи 5 мг прасугрела (у облику хидрохлорида).
- Помоћни састојци су микрокристална целулоза, манитол (Е421), натријум кроскармелоза, хипромелоза (Е464), магнезијум стеарат, лактоза монохидрат, титанијум диоксид (Е171), триацетин (Е1518), црвени гвожђе оксид (само за таблете од 10 мг) (Е172) , жути оксид гвожђа (Е172) и талк.
Како Ефиент изгледа и садржај паковања
Ефиент 10 мг: Таблете су беж боје и облика као двострука стрелица, са утиснутим натписом "10 МГ" на једној страни и "4759" на другој страни.
Ефиент 5 мг: Таблете су жуте и у облику двоструке стрелице, са утиснутом ознаком "5 МГ" на једној страни и "4760" на другој страни.
Ефиент је доступан у паковањима од 14, 28, 30, 56, 84, 90 и 98 таблета.
Не могу се на тржиште ставити све величине паковања.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
ЕФЕКТНЕ 10 МГ ТАБЛЕТЕ ОБЛОЖЕНЕ ФИЛМОМ
02.0 КВАЛИТАТИВНИ И КВАНТИТАТИВНИ САСТАВ
Свака таблета садржи 10 мг прасугрела (у облику хидрохлорида).
Помоћне супстанце са познатим дејством: свака таблета садржи 2,1 мг лактозе.
За потпуну листу помоћних супстанци погледајте одељак 6.1.
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Филмом обложена таблета (таблета).
Таблете у беж боји, двоструке стрелице, са утиснутим натписом "10 МГ" на једној страни и "4759" на другој.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Ефиент, даван у комбинацији са ацетилсалицилном киселином (АСА), индикован је за превенцију атеротромботичних догађаја код одраслих пацијената са акутним коронарним синдромом (АЦС) (тј. Нестабилна ангина пекторис, инфаркт миокарда без елевације СТ сегмента [УА / НСТЕМИ] или СТ-сегмент инфаркт миокарда са повишењем [СТЕМИ]) подвргнут примарној или одложеној перкутаној коронарној интервенцији (ПЦИ).
За даље информације погледајте одељак 5.1.
04.2 Дозирање и начин примене
Дозирање
Одрасли
Ефиент треба започети са појединачном учитавајућом дозом од 60 мг, а затим наставити са 10 мг једном дневно. Пацијенти који узимају Ефиент такође треба да узимају ацетилсалицилну киселину (АСА) 75 мг - 325 мг дневно.
Код пацијената са акутним коронарним синдромом (АЦС) који су подвргнути перкутаној коронарној интервенцији, рано прекидање било ког антитромбоцитног лека, укључујући Ефиент, могло би довести до повећаног ризика од тромбозе, инфаркта миокарда или смрти због пацијентовог основног здравственог стања. Лечење до 12 препоручује се месечно трајање, осим ако је прекид примене лека Ефиент клинички индикован (видети одељке 4.4 и 5.1).
Старосни пацијенти ≥ 75 година
Употреба лека Ефиент код пацијената старијих од 75 година се генерално не препоручује. ≥ 75 година, тада би требало прописати смањену дозу одржавања од 5 мг након пуњења од 60 мг.Пацијенти старији од 75 година имају повећану осетљивост на крварење и повећану изложеност метаболиту активном састојку прасугрела (видети одељке 4.4, 4.8, 5.1 и 5.2).
Пацијенти са телесном тежином
Ефиент треба применити као појединачну учитавајућу дозу од 60 мг, а затим 5 мг једном дневно. Не препоручује се доза одржавања од 10 мг. То је због повећања изложености активном метаболиту прасугрела и повећаног ризика од крварења код пацијената са тежином.
Оштећење бубрега
Није потребно прилагођавање дозе за пацијенте са бубрежном инсуфицијенцијом, укључујући пацијенте са крајњим стадијумом бубрежне болести (видети одељак 5.2). Терапијско искуство код пацијената са бубрежном инсуфицијенцијом је ограничено (видети одељак 4.4).
Оштећење јетре
Није потребно прилагођавање дозе код особа са благим до умереним оштећењем јетре (Цхилд-Пугх класа А и Б) (видети одељак 5.2). Постоји ограничено терапијско искуство код пацијената са благим и умереним оштећењем јетре (видети одељак 4.4). Ефиент је контраиндикован код пацијената са тешким оштећењем јетре (Цхилд Пугх класа Ц).
Педијатријска популација
Безбедност и ефикасност лека Ефиент код деце млађе од 18 година још нису утврђене. Нема доступних података.
Начин примене
За оралну употребу. Ефиент се може давати без обзира на храну. Примена 60 мг учитавајуће дозе прасугрела наташте може довести до бржег дејства лека (видети одељак 5.2). Немојте ломити или ломити таблету.
04.3 Контраиндикације
Преосетљивост на активну супстанцу или било коју помоћну супстанцу наведену у одељку 6.1.
У току је патолошко крварење.
Историјат можданог удара или пролазног исхемијског напада (ТИА).
Тешка дисфункција јетре (Цхилд-Пугх класа Ц).
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Опасност од крварења
У клиничком испитивању фазе 3, кључни критеријуми искључења укључивали су повећан ризик од крварења; анемија; тромбоцитопенија; историја налаза који указују на интракранијалну патологију.
Пацијенти са акутним коронарним синдромом који су подвргнути перкутаној коронарној интервенцији лечени Ефиентом и АСА показали су повећан ризик од већих и мањих крварења према ТИМИ класификационом систему.
Стога, употребу лека Ефиент код пацијената са повећаним ризиком од крварења треба узети у обзир само када се сматра да користи у смислу спречавања исхемијских догађаја надмашују ризик од озбиљног крварења. Ова мера предострожности се посебно односи на пацијенте:
• старији од 75 година (види доле).
• са склоношћу ка крварењу (нпр. Због недавне трауме, недавне операције, недавног или понављајућег гастроинтестиналног крварења или пептичког улкуса у току)
• са телесном тежином
• у истовременом лечењу лековима који могу повећати ризик од крварења, укључујући оралне антикоагуланте, клопидогрел, нестероидне антиинфламаторне лекове (НСАИД) и фибринолитике.
За пацијенте са сталним крварењем који морају да пониште фармаколошке ефекте лека Ефиент, трансфузија тромбоцита може бити одговарајућа.
Давање лека Ефиент пацијентима старијим од 75 година се генерално не препоручује и требало би га чинити само са опрезом након што „пажљива индивидуална процена користи / ризика коју је прописао лекар покаже да су користи од превенције исхемијских догађаја веће од ризика од озбиљног крварења У клиничком испитивању фазе 3, ови пацијенти су имали повећан ризик од крварења, укључујући смртоносно крварење, у поређењу са старијим пацијентима
Терапеутско искуство са прасугрелом је ограничено код пацијената са бубрежном дисфункцијом (укључујући пацијенте са крајњим стадијумом бубрежне болести (ЕСРД)) и код пацијената са умереном дисфункцијом јетре. Ови пацијенти могу имати повећан ризик од крварења.
Због тога, прасугрел треба опрезно користити код ових пацијената.
Пацијенте треба упозорити да приликом узимања прасугрела (у комбинацији са АСА) може да потраје дуже него обично да се заустави крварење и да обавесте свог лекара о сваком необичном крварењу (према локацији или трајању).
Хируршке интервенције
Пре било какве операције и пре узимања новог лека, пацијенти треба да кажу својим лекарима и стоматолозима да узимају прасугрел. Ако пацијент треба да се подвргне изборној операцији, а ефекат против тромбоцита се не сматра одговарајућим, лек Ефиент треба прекинути најмање 7 дана пре операције. Повећана (трострука) учесталост и тежина крварења могу се јавити код пацијената. 7 дана престанка прасугрела (видети одељак 4.8). Користи и ризици прасугрела треба пажљиво размотрити код пацијената код којих анатомија коронарне артерије није дефинисана и могућа је хитна ЦАБГ операција.
Преосјетљивост, укључујући ангиоедем
Реакције преосетљивости, укључујући ангиоедем, забележене су код пацијената који су примали прасугрел, укључујући и пацијенте са историјом реакција преосетљивости на клопидогрел. Препоручује се праћење знакова преосетљивости код пацијената са познатом историјом алергије на тиенопиридине (видети одељак 4.8).
Тромботична тромбоцитопенична пурпура (ПТТ)
ПТТ је пријављен уз употребу прасугрела. ПТТ је озбиљно стање које захтева хитно лечење.
Лактоза
Пацијенти са ретким наследним проблемима интолеранције на галактозу, недостатком Лапп лактазе или малапсорпцијом глукозе-галактозе не би требало да узимају Ефиент..
04.5 Интеракције са другим лековима и други облици интеракција
Варфарин: Истовремена примена Ефиента и деривата кумарина осим варфарина није проучавана. Због могућности повећаног ризика од крварења, потребан је опрез при истовременој примени варфарина (или других деривата кумарина) и прасугрела (видети одељак 4.4).
Нестероидни антиинфламаторни лекови (НСАИД):
Истовремена примена хроничних НСАИЛ није проучавана. Због могућности повећаног ризика од крварења, истовремену примену хроничних НСАИЛ (укључујући инхибиторе ЦОКС-2) и Ефиента треба радити опрезно (видети одељак 4.4).
Ефиент се може давати у комбинацији са лековима који се метаболишу помоћу ензима цитокрома П450 (укључујући статине) или лековима који су индуктори или инхибитори ензима цитокрома П450. Ефиент се такође може давати у комбинацији са АСА, хепарином, дигоксином и лековима који повећавају желудачни пХ, укључујући инхибиторе протонске пумпе и блокаторе Х2.
Иако није предмет посебних студија интеракција, Ефиент је даван у клиничкој студији фазе 3 у комбинацији са хепарином ниске молекулске масе, бивалирудином и инхибиторима ГП ИИб / ИИИа (нема доступних информација о типу инхибитора ГП ИИб / ИИИа користи) без доказа о клинички значајним нежељеним интеракцијама.
Ефекти других лекова на Ефиент:
Ацетилсалицилна киселина: Ефиент се мора давати у комбинацији са АСА. Иако је могућа фармакодинамичка интеракција са АСА са последичним повећањем ризика од крварења, докази о ефикасности и безбедности прасугрела долазе од пацијената лечених у комбинацији са АСА.
Хепарин: Појединачна интравенска болус доза нефракционисаног хепарина (100 У / кг) није значајно променила инхибицију агрегације тромбоцита посредоване прасугрелом. Слично, прасугрел није значајно променио ефекат хепарина на параметре коагулације.
Због тога се оба лека могу примењивати у комбинацији. Повећан ризик од крварења могућ је када се Ефиент даје у комбинацији са хепарином.
Статини: Аторвастатин (80 мг дневно) није променио фармакодинамичку активност прасугрела нити његову инхибицију агрегације тромбоцита, па се не очекује да статини супстрата ЦИП3А утичу на фармакокинетику прасугрела или његову инхибицију агрегације тромбоцита..
Лекови који повећавају пХ желуца: Истовремена примена ранитидина (блокатора Х2) или лансопразола (инхибитора протонске пумпе) дневно није променила АУЦ и Тмак активног метаболита прасугрела, већ је смањила Цмак за 14% и 29%, респективно.У клиничкој студији фазе 3, Ефиент је даван независно од истовремене примене инхибитора протонске пумпе или блокатора Х2. Примена ударне дозе прасугрела од 60 мг без истовремене примене инхибитора протонске пумпе може довести до бржег дејства лека.
Инхибитори ЦИП3АКетоконазол (400 мг дневно), снажан и селективан инхибитор ЦИП3А4 и ЦИП3А5, није променио инхибицију агрегације тромбоцита посредоване прасугрелом или АУЦ и Т активног метаболита прасугрела, али је смањио Цмак 34% на 46% Стога се не очекује да инхибитори ЦИП3А, попут азолних антимикотика, инхибитора ХИВ протеазе, кларитромицина, телитромицина, верапамила, дилтиазема, индинавира, ципрофлоксацина и сока грејпа, имају значајан утицај на фармакокинетику активног метаболита.
Индуктори цитокрома П450: Рифампицин (600 мг дневно), снажан индуктор ЦИП3А и ЦИП2Б6, као и индуктор ЦИП2Ц9, ЦИП2Ц19 и ЦИП2Ц8, није значајно променио фармакокинетику прасугрела. Стога се не очекује да познати индуктори ЦИП3А, попут рифампицина, карбамазепина и других индуктора цитокрома П450, имају значајан утицај на фармакокинетику активног метаболита.
Ефекти Ефиента на друге медицинске производе:
Дигоксин: Прасугрел нема клинички значајан утицај на фармакокинетику дигоксина.
Лекови који се метаболишу помоћу ЦИП2Ц9: Прасугрел није инхибирао ЦИП2Ц9, јер није утицао на фармакокинетику варфарина-С. Због потенцијално повећаног ризика од крварења, потребан је опрез при давању варфарина и Ефиента у комбинацији (видјети дио 4.4).
Лекови који се метаболишу помоћу ЦИП2Б6: Прасугрел је слаб инхибитор ЦИП2Б6. Код здравих испитаника, прасугрел је смањио изложеност хидроксибупропиону, метаболиту бупропиона посредованом ЦИП2Б6, за 23%. Овај ефекат ће вероватно изазвати клиничку забринутост само ако се прасугрел примењује у комбинацији са лековима за које је ЦИП2Б6 једини метаболички пут и који имају ограничен терапијски оквир (нпр. Циклофосфамид, ефавиренз).
04.6 Трудноћа и дојење
Нису спроведене клиничке студије код трудница или дојиља.
Трудноћа
Студије на животињама не указују на директне штетне ефекте на трудноћу, ембрионални / фетални развој, пород или постнатални развој (видети одељак 5.3). С обзиром да студије о репродуктивној активности на животињама не предвиђају увек ефекте на људе, Ефиент би требало користити у трудноћи само ако потенцијална корист оправдава потенцијални ризик за фетус.
Време храњења
Није познато да ли се прасугрел излучује у мајчино млеко. Студије на животињама показале су елиминацију прасугрела у мајчином млеку, па се не препоручује употреба прасугрела током дојења.
Плодност
Прасугрел није имао ефекта на мушку и женску плодност код пацова изложених оралним дозама до 240 пута веће од препоручене дневне дозе за одржавање одржаване код људи (процењене у мг / м2).
04.7 Утицај на способност управљања возилима и машинама
Не очекује се да Прасугрел утиче или занемарљиво утиче на способност управљања возилима и рада на машинама.
04.8 Нежељени ефекти
Сажетак сигурносног профила
Безбедност код пацијената са акутним коронарним синдромом који су били подвргнути перкутаној коронарној интервенцији процењена је у клиничком испитивању клопидогрелом (ТРИТОН) у коме је 6.741 пацијент лечен прасугрелом (са учитавајућом дозом од 60 мг и дозом одржавања од 10 мг дневно) медијана 14,5 месеци (5.802 пацијената лечено је дуже од 6 месеци, 4.136 пацијената лечено више од 1 године). Стопа укидања испитиваног лека због нежељених догађаја била је 7,2% за прасугрел и 6,3% за клопидогрел. Од ових, крварење је била најчешћа нежељена реакција која је довела до прекида терапије испитиваним лековима за оба лека (2,5% за прасугрел и 1,4% за клопидогрел).
Крварење
Крварење које није повезано са премосницом коронарне артерије (ЦАБГ)
У студији ТРИТОН учесталост пацијената који су доживели епизоду крварења која није повезана са премосницом коронарне артерије (ЦАБГ) приказана је у Табели 1. Учесталост великог крварења (према дефиницијама ТИМИ) која није повезана са премошћавањем коронарне артерије (ЦАБГ), укључујући оне у ризику од смрти и фаталног исхода, као и код мањег крварења (према дефиницијама ТИМИ), било је статистички значајно веће код испитаника лечених прасугрелом у поређењу са субјектима који су примали клопидогрел код оболелих од УА / НСТЕМИ него код целе АЦС популације . Нису уочене значајне разлике у популацији СТЕМИ. Најчешће место спонтаног крварења био је гастроинтестинални тракт (1,7% са прасугрелом и 1,3% са клопидогрелом); најчешће место изазваног крварења било је место приступа артеријама (1,3% са прасугрелом и 1,2% са клопидогрелом).
Табела 1: Учесталост крварења која није повезана са хирургијом премоснице коронарних артерија (ЦАБГ) а (% пацијената)
а Догађаји дефинисани критеријумима тромболизе студијске групе за инфаркт миокарда (ТИМИ) који се процењују централизовано.
б Друге стандардне терапије су примењиване према потреби.
ц Било које интракранијално крварење или било које клинички евидентно крварење повезано са смањењем хемоглобина ≥5 г / дл.
д Крварење под ризиком од смрти је подгрупа великог крварења (према ТИМИ дефиницијама) е укључује доле наведене типове. Пацијенти се могу бројати у више од једног реда.
и ИЦХ = интракранијално крварење.
ф Клинички евидентно крварење повезано са смањењем хемоглобина ≥3 г / дл, али
Старосни пацијенти ≥ 75 година
Стопе великог или мањег крварења (ТИМИ) које нису повезане са премосницом коронарне артерије (ЦАБГ):
* ТРИТОН студија код пацијената са АЦС -ом на ПЦИ
** ТРИЛОГИ-АЦС студија код пацијената који нису подвргнути ПЦИ (видети одељак 5.1):
до прасугрел 10 мг; прасугрел 5 мг ако
Пацијенти са телесном тежином
Стопе великог или мањег крварења (ТИМИ) које нису повезане са премосницом коронарне артерије (ЦАБГ):
* ТРИТОН студија код пацијената са АЦС -ом на ПЦИ
** ТРИЛОГИ-АЦС студија код пацијената који нису подвргнути ПЦИ (видети одељак 5.1):
до прасугрел 10 мг; прасугрел 5 мг ако је стар ≥75 година
Пацијенти тежине ≥60 кг и старости
Код пацијената тежине ≥60 кг и старост
Крварење повезано са премосницом коронарне артерије (ЦАБГ)
У клиничком испитивању фазе 3, 437 пацијената је подвргнуто премосници коронарне артерије (ЦАБГ). Од ових пацијената, стопа великог или мањег крварења (ТИМИ) у вези са премошћавањем коронарне артерије (ЦАБГ) била је 14,1% за групу прасугрела и 4,5% за групу са клопидогрелом. Највећи ризик од епизода крварења код испитаника лечених прасугрелом трајао је до 7 дана након последње дозе испитиваног лека. За пацијенте који су примили тиенопиридин у року од 3 дана пре премошћавања коронарне артерије (ЦАБГ), стопе великог или мањег крварења (ТИМИ) биле су 26,7% (12 од 45 пацијената) у групи прасугрела., У поређењу са 5,0% (3 од 60 пацијената) у групи која је примала клопидогрел.За пацијенте који су примили последњу дозу тиенопиридина у року од 4 до 7 дана пре премошћавања коронарне артерије (ЦАБГ), учесталост се смањила на 11,3% (9 од 80 пацијената) у групи прасугрела и 3,4 % (3 од 89 пацијената) у групи која је примала клопидогрел.Више од 7 дана након престанка узимања, примећене стопе крварења повезане са премосницом коронарне артерије (ЦАБГ) биле су сличне између две групе лечења (видети одељак 4.4).
Збирна табела нежељених реакција
Табела 2 резимира хеморагијске и нехеморагичне нежељене реакције у студији ТРИТОН, или из спонтаних извештаја, класификованих према учесталости и по органима система. Њихова учесталост је дефинисана помоћу следећих конвенција: Веома честе (≥ 1/10); честе (≥ 1/100,
Табела 2: Хеморагијске и нехеморагичне нежељене реакције
Код пацијената са или без историје пролазног исхемијског напада (ТИА) или можданог удара, учесталост можданог удара у студији фазе 3 била је следећа (видети одељак 4.4):
* ИЦХ = интракранијално крварење.
Пријављивање сумње на нежељене реакције
Извештавање о сумњи на нежељене реакције које се јаве након добијања дозволе за лек важно је јер омогућава континуирано праћење односа користи и ризика лека. Од здравствених радника се тражи да пријаве све сумње на нежељене реакције путем националног система за пријављивање. У „Анексу В .
04.9 Предозирање
Предозирање Ефиент -ом може довести до продуженог времена крварења и последичних компликација крварења. Нема података о "отказивању" фармаколошке активности прасугрела; међутим, када је потребна брза корекција продуженог времена крварења, може се размотрити трансфузија тромбоцита или других продуката крви.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: лекови против тромбоцита, искључујући хепарин.
АТЦ код: Б01АЦ22.
Фармакодинамички ефекти
Прасугрел је инхибитор активације и агрегације тромбоцита који делује путем неповратног везивања његовог активног метаболита за рецепторе АДП тромбоцита класе П2И12. Функција тромбоцита може довести до смањења учесталости кардиоваскуларних догађаја као што су смрт, инфаркт миокарда или мождани удар.
Након учитавајуће дозе од 60 мг прасугрела, инхибиција агрегације тромбоцита изазвана АДП-ом јавља се 15 минута са 5 мцМ АДП-а и 30 минута са 20 мцМ АДП-а. Максимална инхибиција агрегације тромбоцита индукована АДП-ом добијена прасугрелом је 83% са 5 мцМ АДП и 79% са 20 мцМ АДП, у оба случаја са 89% здравих испитаника и пацијената са стабилном атеросклерозом достижући најмање 50% инхибиције агрегације тромбоцита у року од 1 сата. Инхибиција агрегације тромбоцита постигнута са Прасугрелом показује смањену међу- (9%) и интра-индивидуалну (12%) варијабилност са 5 мцМ и 20 мцМ АДП. Просечна инхибиција агрегације тромбоцита у равнотежи била је 74% и 69%, са 5 мцМ АДП и 20 мцМ АДП, респективно, и постигнута је након периода од 3 до 5 дана примене појединачне дозе. мг прасугрела којем је претходила учитавајућа доза од 60 мг.Преко 98% испитаника имало је ≥ 20% инхибиције агрегације тромбоцита током дозе одржавања.
Након третмана, агрегација тромбоцита се постепено враћала на почетну вредност у периоду од 7 до 9 дана након примене појединачне учитавајуће дозе од 60 мг прасугрела и преко 5 дана након престанка дозирања одржавања равнотеже.
Подаци о преласку са клопидогрела на прасугрелНакон примене клопидогрела 75 мг једном дневно током 10 дана, 40 здравих испитаника је прешло на прасугрел 10 мг једном дневно, са или без пуњења 60 мг. Слична или већа инхибиција агрегације тромбоцита примећена је код прасугрела. Прелазак директно на 60 мг учитавајуће дозе прасугрела резултирао је бржим почетком веће инхибиције тромбоцита. Након примене оптерећујуће дозе од 900 мг клопидогрела (у комбинацији са АСА) , 56 испитаника са АЦС -ом је 14 дана лечено прасугрелом 10 мг једном дневно или 150 мг клопидогрелом једном дневно, а затим је прошло терапију преласком на клопидогрел у дози од 150 мг или 10 мг прасугрела у наредних 14 дана („пребацивање“).Највећа инхибиција агрегације тромбоцита примећена је код пацијената који су прешли на 10 мг прасугрела у поређењу са онима који су лечени 150 мг клопидогрела.У студији на 276 пацијената са АЦС -ом који су били подвргнути ПЦИ, прелазећи са почетне оптерећујуће дозе од 600 мг клопидогрела или плацеба, узимајући при пријему у болницу, пре коронарне ангиографије, при учитавајућој дози од 60 мг прасугрела дате у време перкутане коронарне интервенције, резултирало је сличним повећањем броја инхибиторних тромбоцита у агрегацији током трајања 72-часовне студије.
Ефикасност и безбедност у акутном коронарном синдрому
У студији ТРИТОН фазе 3, Ефиент (прасугрел) је упоређен са клопидогрелом, оба дата у комбинацији са АСА и другим стандардним терапијама. ТРИТОН је међународна, рандомизирана, двоструко слијепа, паралелна, мултицентрична студија која је обухватила 13.608 пацијената. Пацијенти су имали АЦС са умереним до високим ризиком од УА и НСТЕМИ или СТЕМИ и лечени су ПЦИ.
Пацијенти са УА / НСТЕМИ у року од 72 сата од почетка симптома или са СТЕМИ од 12 сати до 14 дана од почетка симптома, рандомизирани су након сазнања о анатомији коронарне циркулације. Пацијенти са СТЕМИ у року од 12 сати од почетка симптома и заказани за примарну ПЦИ могу се насумично насумично одредити без знања о коронарној слици.
Пацијенти рандомизовани на прасугрел (60 мг учитавајуће дозе праћене са 10 мг једном дневно) или клопидогрела (300 мг учитавајуће дозе праћене 75 мг једном дневно) лечени су просечно 14,5 месеци (максимално 15 месеци са минималним од 6 месеци праћења). Пацијенти су такође примали АСА (75 мг до 325 мг једном дневно).
Коришћење било ког тиенопиридина 5 дана пре уписа био је критеријум за искључење. Друге терапије, као што су хепарин и инхибитори ГПИИб / ИИИа, примењиване су по нахођењу лекара. Приближно 40% пацијената (у свакој терапијској групи) примало је инхибиторе ГПИИб / ИИИа за подршку ПЦИ (нема доступних информација о типу ГП ИИб / Употребљен је инхибитор ИИИа.) Приближно 98% пацијената (у свакој терапијској групи) је директно примало антитромбине (хепарин, хепарин ниске молекулске масе, бивалирудин или други лек) као подршку ПЦИ.
Примарна мера исхода студије било је време до појаве првог догађаја кардиоваскуларне (ЦВ) смрти, нефаталног инфаркта миокарда (МИ) или нефаталног можданог удара. Сложена циљна анализа у целој популацији АЦС (укључујући групе УА / НСТЕМИ и СТЕМИ) била је условљена демонстрацијом статистичке супериорности прасугрела над клопидогрелом у групи УА / НСТЕМИ (стр.
Укупна популација АЦС -а: Ефиент је показао супериорну ефикасност у односу на клопидогрел у смањењу примарне композитне крајње тачке, као и унапред одређених секундарних крајњих тачака, укључујући тромбозу стента (видети Табелу 3). Корист од прасугрела била је евидентна у прва 3 дана и наставила се до краја студије. Врхунска ефикасност праћена је повећањем великог крварења (видети одељке 4.4 и 4.8). Популација пацијената била је 92% белаца, са 26% жена и 39% у доби ≥ 65 година. Користи повезане са прасугрелом биле су независне од употребе других акутних и дуготрајних кардиоваскуларних терапија, укључујући хепарин / хепарин ниске молекулске масе, бивалирудин, интравенозне инхибиторе ГПИИб / ИИИа, лекове за снижавање липида, бета-блокаторе и инхибиторе ензима ангиотензина. Ефикасност прасугрела није зависила од дозе АСА (75-325 мг једном дневно). Употреба оралних антикоагуланса, лекова против тромбоцита осим оних који се проучавају, и хроничних НСАИД-а није била дозвољена у студији ТРИТОН. У укупној популацији АЦС-а, прасугрел је био повезан са мањом учесталошћу ЦВ смрти. нефаталног можданог удара у поређењу са клопидогрелом, без обзира на основне карактеристике као што су старост, пол, телесна тежина, географска регија, употреба инхибитора ГПИИб / ИИИа и врста стента. Корист је углавном последица значајног смањења нефаталних Случајеви АМИ (видети Табелу 3) Дијабетичари су показали значајно смањење примарних и свих секундарних композитних крајњих тачака.
Корист прасугрела примећена код пацијената старијих од 75 година била је мања од оне која је примећена код пацијената са дијабетесом, СТЕМИ -јем, повећаним ризиком од тромбозе стента или понављајућим догађајима.
Пацијенти са историјом ТИА или са исхемијским нападом у историји старијим од 3 месеца пре терапије прасугрелом нису имали смањење примарног композитног циља.
Табела 3: Пацијенти са клиничким исходима у примарној анализи студије ТРИТОН
У укупној популацији АЦС -а, анализа сваке од секундарних крајњих тачака показала је значајну корист (стр
Прасугрел је био повезан са смањењем тромбозе стента за 50% током периода праћења од 15 месеци. Смањење тромбозе стента са Ефиент -ом је примећено и рано и после 30 дана и за металне и за медицинске стентове.
У анализи пацијената који су преживели исхемијски догађај, прасугрел је био повезан са смањењем учесталости накнадних примарних крајњих догађаја (7,8% са прасугрелом наспрам 11,9% са клопидогрелом).
Иако је крварење повећано прасугрелом, сложена "анализа циља" која се састоји од смрти из свих узрока, нефаталног инфаркта миокарда, нефаталног можданог удара и великог крварења повезаног са ТИМИ-ом без ЦАБГ-а била је повољна за Ефиент у односу на клопидогрел (ХР 0,87 ; 95% ЦИ, 0,79 до 0,95; п = 0,004). У студији ТРИТОН, на сваких 1.000 пацијената лечених Ефиентом, било је 22 мање пацијената са инфарктом миокарда, и још 5 са великим крварењем које није повезано са ЦАБГ, у поређењу са пацијентима леченим клопидогрелом.
Резултати фармакодинамичке / фармакогеномске студије на 720 азијских пацијената са АЦС -ом који су прошли ПЦИ показали су да се са прасугрелом постиже виши ниво инхибиције тромбоцита него са клопидогрелом, те да је доза одржавања прасугрела од 60 мг / 10 мг одговарајући режим дозирања код азијских испитаника који теже имају најмање 60 кг и имају мање од 75 година (видети одељак 4.2).
У 30-месечној студији (ТРИЛОГИ-АЦС), спроведеној на 9326 медицински лечених пацијената са АЦС УА / НСТЕМИ, без реваскуларизације (нерегистрована индикација), прасугрел није значајно смањио учесталост композитне ЦВ смртне смрти од ИМ, или можданог удара Стопе великог крварења (ТИМИ) (укључујући ризик од смрти, смртног исхода и интракранијалног крварења) биле су сличне код пацијената лечених прасугрелом и клопидогрелом. ≥ 75 година или тежине мање од 60 кг (Н = 3022) биле су рандомизовано на прасугрел 5 мг.Као и код старијих пацијената
05.2 Фармакокинетичка својства
Прасугрел је пролек и брзо се метаболише ин виво активном метаболиту и неактивним метаболитима. Изложеност активном метаболиту (АУЦ) има умерену до ниску варијабилност међу субјектима (27%) и унутар субјекта (19%). Фармакокинетика прасугрела је слична код здравих испитаника, пацијената са стабилном атеросклерозом и пацијената на перкутаној коронарној интервенцији.
Апсорпција
Апсорпција и метаболизам прасугрела су брзи, са највећом концентрацијом активног метаболита у плазми (Цмак) која се достиже за приближно 30 минута. Изложеност активном метаболиту (АУЦ) пропорционално се повећава у односу на терапијску дозу. У једној студији на здравим субјектима, АУЦ од активни метаболит није промењен оброком са високим процентом масти и калорија, али је Цмак смањен за 49%, а време постизања Цмак (Тмак) повећано је са 0, 5 на 1,5 сати. У студији ТРИТОН, Ефиент је даван без обзира на храну, па се Ефиент може давати без обзира на храну; међутим, примена почетне дозе прасугрела наташте може довести до бржег дејства (видети одељак 4.2).
Дистрибуција
Везивање активног метаболита за хумани серумски албумин (4% раствор пуфера) било је 98%.
Метаболизам
Прасугрел се не појављује у плазми након оралне примене. Брзо се хидролизује у цревима у тиолактон, који се затим у једном метаболичком кораку претвара у активни метаболит цитокромом П450, углавном ЦИП3А4 и ЦИП2Б6 и у мањој мери ЦИП2Ц9 и ЦИП2Ц19. Активни метаболит се затим метаболише у два једињења неактиван С-метилацијом или коњугацијом са цистеином.
Код здравих испитаника, пацијената са стабилном атеросклерозом и пацијената са АЦС који су примали Ефиент, није било значајног утицаја генетске варијације ЦИП3А5, ЦИП2Б6, ЦИП2Ц9 или ЦИП2Ц19 на фармакокинетику прасугрела или његову инхибицију агрегације тромбоцита.
Елиминација
Отприлике 68% дозе прасугрела се елиминише урином, а 27% фецесом као неактивни метаболити. Полувреме елиминације активног метаболита је приближно 7,4 сата (2 до 15 сати).
Посебне популације:
Старији грађани: У студији на здравим субјектима између 20 и 80 година, старост није имала значајан утицај на фармакокинетику прасугрела или инхибицију агрегације тромбоцита коју производи. У „великој фази 3 клиничког испитивања“, изложеност активном метаболиту (АУЦ) била је 19% већа код врло старијих пацијената (старости ≥ 75 година) у поређењу са испитаницима старости
Прасугрел треба користити опрезно код пацијената старијих од 75 година због могућег ризика од крварења у овој популацији (видети одељке 4.2 и 4.4). У студији на субјектима са стабилном атеросклерозом, средња изложеност (АУЦ) активном метаболиту код пацијената старијих од 75 година који су узимали 5 мг прасугрела била је приближно упола мања него код пацијената старијих од 75 година.
Хепатична инсуфицијенција: Није потребно прилагођавање дозе за пацијенте са благим до умереним оштећењем јетре (Цхилд-Пугх класа А или Б). Фармакокинетика прасугрела и његова инхибиција агрегације тромбоцита били су слични код испитаника са благим до умереним оштећењем јетре у поређењу са здравим субјектима. Фармакокинетика и фармакодинамика прасугрела код пацијената са тешким оштећењем јетре нису проучавани. Не сме се користити код пацијената са тешко оштећење јетре (видети одељак 4. 3).
Инсуфицијенција бубрега: Није потребно прилагођавање дозе за пацијенте са бубрежном инсуфицијенцијом, укључујући пацијенте са крајњим стадијумом бубрежне болести (ЕСРД). Фармакокинетика прасугрела и његова инхибиција агрегације тромбоцита су слични код пацијената са умереним оштећењем бубрега (брзина гломеруларне филтрације (ГФР) 30-2)) и код здравих испитаника. Инхибиција агрегације тромбоцита посредована прасугрелом била је слична. Такође код пацијената са ЕСРД којима је потребна хемодијализа у поређењу са здравим субјектима, иако су се Цмак и АУЦ активног метаболита смањиле за 51% односно 42% код пацијената са ЕСРД.
Телесне тежине: Изложеност активног метаболита (АУЦ) прасугрела је приближно 30 до 40% већа код здравих испитаника и пацијената са телесном тежином
Етничка припадност: У клиничким фармаколошким студијама, након прилагођавања телесне тежине, АУЦ активног метаболита била је приближно 19% већа код испитаника из Кине, Јапана и Кореје у поређењу са белцима, углавном у односу на већу изложеност код азијских испитаника са телесном тежином
Пол: Код здравих испитаника и пацијената, фармакокинетика прасугрела код жена и мушкараца је слична.
Педијатријска популација: Фармакокинетика и фармакодинамика прасугрела нису испитиване у педијатријској популацији (видети одељак 4.2).
05.3 Предклинички подаци о безбедности
Неклинички подаци нису открили никакав посебан ризик за људе на основу конвенционалних студија фармакологије безбедности, токсичности при поновљеним дозама, генотоксичности, канцерогеног потенцијала или токсичности за репродукцију. Ефекти у неклиничким студијама су примећени. Само при изложености која се сматра довољном већом од максимална изложеност људи што указује на ниску релевантност за клиничку употребу.
Токсиколошке студије о развоју ембрија и фетуса код пацова и зечева нису показале доказе о малформацијама узрокованим прасугрелом. При веома високим дозама (> 240 пута већа од препоручене дневне дозе одржавања за људе у мг / м2) која је изазвала ефекте на телесну тежину мајке и / или унос хране, дошло је до благог смањења телесне тежине код потомака (у поређењу са контролом).У пре- и постнаталним студијама на пацовима, лечење мајке није имало ефекта на бихејвиорални или репродуктивни развој потомака у дозама до 240 пута веће од препоручене дневне дозе за одржавање одржаване код људи (изражене у мг / м2).
Нису уочени тумори повезани са једињењима у двогодишњој студији на пацовима са изложеношћу прасугрелу у распону већим од 75 пута од препоручене терапијске изложености код људи (на основу изложености хумане плазме активном метаболиту и људским метаболитима). Главни у циркулацији). Код мишева који су 2 године били изложени високим дозама (> 75 пута већа од изложености људи) дошло је до "повећане учесталости тумора (хепатоцелуларни аденоми), али се то сматрало секундарним у односу на индукцију ензима индукованог прасугрелом. Л" Повезаност јетре специфична за глодаре тумори и индукција ензима изазваних лековима добро су документовани у литератури. Повећање тумора јетре уз примену прасугрела код мишева не сматра се релевантним ризиком за људе.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Језгро таблета:
Микрокристална целулоза
Манитол (Е421)
Натријум кроскармелоза
Хипромелоза (Е464)
Магнезијум стеарат
Премазивање:
Лактоза монохидрат
Хипромелоза (Е464)
Титанијум диоксид (Е171)
Триацетин (Е1518)
Црвени оксид гвожђа (Е172)
Жути оксид гвожђа (Е172)
Талц
6.2 Некомпатибилност
Није применљиво.
06.2 Некомпатибилност
2 године.
06.3 Период важења
2 године.
06.4 Посебне мере предострожности при складиштењу
Овај лек не захтева посебне температуре складиштења. Чувати у оригиналном паковању ради заштите од ваздуха и влаге.
06.5 Природа непосредног паковања и садржај паковања
Алуминијумски блистер у кутијама од 14, 28, 30, 30 (к1), 56, 84, 90 (к1) и 98 таблета.
Не могу се на тржиште ставити све величине паковања.
06.6 Упутства за употребу и руковање
Нема посебних упутстава.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
Ели Лилли Недерланд БВ, Гроотслаг 1-5, НЛ-3991 РА Хоутен, Холандија.
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
ЕУ/1/08/503/008
039055088
ЕУ/1/08/503/009
039055090
ЕУ/1/08/503/010
039055102
ЕУ/1/08/503/011
039055114
ЕУ/1/08/503/012
039055126
ЕУ/1/08/503/013
039055138
ЕУ/1/08/503/014
039055140
ЕУ/1/08/503/016
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: 25. фебруар 2009
Последњи датум обнове:
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
11.0 ЗА РАДИО ДРОГЕ, ПОТПУНИ ПОДАЦИ О ДОСИМЕТРИЈИ ИНТЕРНОГ ЗРАЧЕЊА
12.0 ЗА РАДИО -ЛИЈЕКОВЕ, ДОДАТНА ДЕТАЉНА УПУТСТВА О ПРИМЕРНОЈ ПРИПРЕМИ И КОНТРОЛИ КВАЛИТЕТА
ДОГОВОРЕНО СА ЕВРОПСКОМ МЕДИЦИНСКОМ АГЕНЦИЈОМ (ЕМА) И ИТАЛИЈАНСКОМ АГЕНЦИЈОМ ЗА ДРОГЕ (АИФА)
Децембар 2013
Повећан ризик од тешког крварења код пацијената са нестабилном ангином / инфарктом миокарда са повећањем сегмента СТ (УА) / НСТЕМИ када се пре дијагностичке коронарне ангиографије примењује ЕФИЕНТ (прасугрел).
Поштовани докторе, драги докторе,
„Европска агенција за лекове и Италијанска агенција за лекове - АИФА, у договору са Даиицхи -Санкио и Ели Лилли Италиа, желе да вас информишу о следећој препоруци у вези са употребом ЕФИЕНТ -а (прасугрела), антиагрегацијског лека назначеног за лечење акутног коронарни синдром (АЦС) код пацијената на перкутаној коронарној интервенцији (ПЦИ):
Код пацијената са нестабилном ангином / инфарктом миокарда са повишењем СТ сегмента (УА) / НСТЕМИ, када се коронарна ангиографија изводи у року од 48 сати од хоспитализације, учитавајућу дозу ЕФИЕНТ-а треба дати само у време ПЦИ-а како би се ризик свео на минимум. крварења.
Ова препорука се заснива на резултатима недавно завршене клиничке студије код пацијената са НСТЕМИ која је заказана за коронарографију 2 до 48 сати након рандомизације. Студија је упоредила ефекте примене почетне оптерећујуће дозе прасугрела од 30 мг пре коронарне ангиографије (у просеку 4 сата), након чега је уследила „додатна доза од 30 мг у време ПЦИ, са ефектом насталим након примене пуне учитавајућа доза од 60 мг у време ПЦИ. Резултати су показали већи ризик од крварења повезаног са употребом почетне оптерећујуће дозе пре коронарне ангиографије, праћене додатном дозом у време ПЦИ у поређењу са једном пуном дозом прасугрела у време ПЦИ. Није било разлике у ефикасности примећено између два режима дозирања.
Студија "АЦЦОАСТ" под насловом: Поређење Прасугрела у време перкутане коронарне интервенције или као предтретман у време дијагнозе код пацијената са инфарктом миокарда без елевације СТ.
Сазнајте више о безбедносним аспектима
АЦЦОАСТ је била 30-дневна студија спроведена на 4.033 пацијената са НСТЕМИ и повишеним тропонином који су требали бити подвргнути коронарној ангиографији, а затим ПЦИ 2 до 48 сати након рандомизације. Субјекти који су примали оптерећујућу дозу прасугрела од 30 мг у просеку 4 сата пре коронарне ангиографије, праћену оптерећујућом дозом од 30 мг у време ПЦИ (н = 2037), имали су повећан ризик од перипроцедуралног крварења. (није у вези са операцијом премоснице коронарне артерије) и нема додатне користи у поређењу са пацијентима који су примали оптерећујућу дозу од 60 мг у време ПЦИ (н = 1996). Конкретно, учесталост композитне мете кардиоваскуларне смрти, инфаркта миокарда, можданог удара, хитне реваскуларизације или употребе инхибитора гликопротеина (ГП) ИИб / ИИИа „у терапији спасавања“ у року од 7 дана од рандомизације није значајно смањена код испитаника који су примали прасугрел пре коронарне ангиографије у поређењу са пацијентима који су примали пуну оптерећујућу дозу прасугрела у време ПЦИ. Штавише, учесталост главног безбедносног циља, представљена свим великим крварењима према ТИМИ (ЦАБГ и нон-ЦАБГ догађаји) у року од 7 дана од рандомизације код свих лечених испитаника, била је значајно већа код испитаника који су примали прасугрел у две подељене дозе (4 сати пре коронарне ангиографије и у време ПЦИ), у поређењу са пацијентима који су примали пуну оптерећујућу дозу прасугрела у једној примени у време ПЦИ.
Пријављивање сумњивих нежељених реакција
Лекари и други здравствени радници морају да пријаве сваку сумњу на нежељене реакције повезане са лековима који садрже прасугрел.
Лекари и други здравствени радници морају, по закону, слати извештаје о сумњи на нежељене реакције, користећи посебан папирни образац (доступан на веб страници хттп://ввв.агензиафармацо.гов.ит/ситес/дефаулт/филес/типо_филецб84.пдф) или попуњавањем електронског обрасца на мрежи (хттп://ввв.агензиафармацо.гов.ит/ситес/дефаулт/филес/сцхеда_аифа_опер_санитарио16.07.2 012.доц) одмах, управнику фармаковигиланције здравствене установе којој припадају или , ако послују у приватним здравственим установама, преко Одељења за здравље, менаџеру фармаковигиланце АСЛ -а надлежном за то подручје.
Додатне информације
За питања и / или додатне информације, обратите се канцеларији Ели Лилли за медицинске информације позивом на следећи бесплатни број: 800117678 или писањем на следећу адресу: мединфоита@лилли.цом
Извештаји о сумњи на нежељене реакције лекова морају се послати шефу фармаковигиланције структуре којој Оператер припада.
Ова Информативна белешка је такође објављена на веб страници АИФА -е (ввв.агензиафармацо.ит) чије се редовне консултације препоручују за најбоље стручне и услужне информације грађанима.