Активни састојци: Трастузумаб
Херцептин 150 мг прашак за концентрат за раствор за инфузију
Улошци за паковање Херцептин доступни су за величине паковања:- Херцептин 150 мг прашак за концентрат за раствор за инфузију
- Херцептин 600 мг раствор за ињекције у бочици
- Херцептин 600 мг раствор за ињекције путем уређаја за администрацију
Зашто се користи Херцептин? За шта је то?
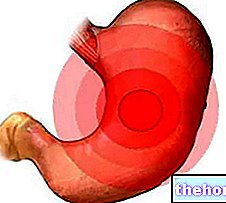
Херцептин садржи активну супстанцу трастузумаб, која је моноклонско антитело. Моноклонска антитела се везују за специфичне протеине или антигене. Трастузумаб је дизајниран да се селективно веже за антиген назван рецептор 2 хуманог епидермалног фактора раста (ХЕР2). ХЕР2 је присутан у великим количинама на површини неких ћелија рака, стимулишући њихов раст. Када се Херцептин веже за ХЕР2, он зауставља раст ових ћелија и доводи до њихове смрти.
Ваш лекар може прописати Херцептин за лечење рака дојке и желуца ако:
- Имате рани стадијум рака дојке са високим нивоом протеина званог ХЕР2.
- Имате метастатски рак дојке (рак дојке који се проширио далеко од примарног тумора) са високим нивоом ХЕР2. Херцептин се може прописати у комбинацији са кемотерапијским лијековима паклитакселом или доцетакселом као први лијек за метастатски рак дојке или се може прописати сам ако су се други третмани показали недјелотворнима. Такође се користи у комбинацији са лековима који се зову инхибитори ароматазе за лечење пацијената са високим нивоом ХЕР2 и метастатским раком дојке позитивним на хормонске рецепторе (рак који је осетљив на присуство женских полних хормона).
- Имате метастатски рак желуца са високим нивоом ХЕР2, у комбинацији са другим лековима против рака, капецитабином или 5-флуороурацилом и цисплатином.
Контраиндикације Када се Херцептин не сме користити
Немојте користити Херцептин ако:
- ако сте алергични на трастузумаб, мишје (мишје) протеине или на било који други састојак.
- имате тешке проблеме са дисањем у мировању због рака или ако вам је потребан третман кисеоником.
Предострожности при употреби Шта треба да знате пре него што узмете Херцептин
Ваш лекар ће пажљиво надзирати вашу терапију.
Срчани преглед
Лечење Херцептином самостално или са таксаном може утицати на ваше срце, посебно ако сте већ узимали „антрациклин (таксани и антрациклини су две друге врсте лекова који се користе за лечење рака). Стога ће се ваша функција срца прво проверити., Током (свака три месеца) и након (до две до пет година) лечења Херцептином Ако осетите знакове срчане инсуфицијенције (тј. срце не пумпа крв правилно), можда ћете морати да престанете са узимањем Херцептина.
Разговарајте са својим лекаром, фармацеутом или медицинском сестром пре него што узмете Херцептин ако:
- сте имали срчану инсуфицијенцију, коронарну артеријску болест, болест срчаних залистака (шум на срцу), висок крвни притисак, узимали сте или тренутно узимате било које лекове за лечење високог крвног притиска.
- сте узимали или тренутно узимате лекове који се зову доксорубицин или епирубицин (лекови који се користе за лечење рака). Ови лијекови (или било који други антрациклин) могу оштетити срчани мишић и повећати ризик од срчаних проблема при узимању Херцептина.
- патите од недостатка ваздуха, посебно ако тренутно узимате таксан. Херцептин може изазвати потешкоће у дисању, посебно први пут када се даје. Ово може бити озбиљније ако већ патите од недостатка ваздуха. Врло ретко су пацијенти са тешким тешкоћама дисања пре лечења умирали када су примали Херцептин.
- су икада примали друге лекове за лечење рака.
Ако примате Херцептин у комбинацији са било којим другим лековима који се користе за лечење рака, као што су паклитаксел, доцетаксел, инхибитор ароматазе, капецитабин, 5-флуороурацил или цисплатин, требало би да прочитате и упутство за употребу ових лекова.
Деца и адолесценти
Херцептин се не препоручује млађима од 18 година.
Интеракције Који лекови или храна могу променити ефекат Херцептина
Обавестите свог лекара, фармацеута или медицинску сестру ако узимате, недавно сте узимали или бисте могли да узмете било који други лек.
Може проћи и до 7 месеци док се Херцептин не избаци из тела. Због тога би требало да кажете свом лекару, фармацеуту или медицинској сестри да сте узели Херцептин ако започнете нове лекове у року од 7 месеци од престанка терапије.
Упозорења Важно је знати да:
Трудноћа
- Ако сте трудни, мислите да сте трудни или планирате трудноћу, обавестите свог лекара, фармацеута или медицинску сестру пре него што узмете овај лек.
- Морате користити ефикасну контрацепцију током лечења Херцептином и најмање 7 месеци након престанка лечења.
- Ваш лекар ће разговарати са вама о ризицима и користима узимања Херцептина током трудноће.У ретким случајевима, примећено је смањење (амнионске) течности која окружује бебу у развоју у материци код трудница које су лечене Херцептином. Ово стање би могло бити штетно за бебу у материци и било је повезано с непотпуним сазријевањем плућа, што је резултирало феталном смрћу.
Време храњења
Немојте дојити док узимате Херцептин и 7 месеци након последње дозе Херцептина, јер Херцептин може проћи беби преко мајчиног млека. Питајте свог лекара или фармацеута за савет пре него што узмете било који лек.
Вожња и управљање машинама
Није познато да ли ће Херцептин утицати на вашу способност управљања возилима и рада на машинама. Међутим, ако осетите симптоме попут зимице или грознице, не треба да возите или управљате машинама док ти симптоми не нестану.
Дозирање и начин употребе Како користити Херцептин: Дозирање
Пре почетка лечења, ваш лекар ће одредити количину ХЕР2 у вашем тумору. Само пацијенти са повишеним нивоом ХЕР2 биће лечени Херцептином. Херцептин треба давати само лекар или медицинска сестра. Ваш лекар ће прописати одговарајућу дозу и распоред лечења. Доза Херцептина зависи од ваше телесне тежине.
Постоје две различите врсте (формулације) Херцептина:
- један се даје инфузијом у вену (интравенозна инфузија)
- други се даје ињекцијом испод коже (поткожна ињекција).
Важно је проверити етикету производа како бисте били сигурни да се примењује исправна формулација коју је прописао ваш лекар. Херцептин интравенозна формулација није намењена за поткожну примену и треба се примењивати само интравенозном ињекцијом.
Херцептин интравенозна формулација се примењује као "интравенозна инфузија (" капање ") директно у вене. Прва доза вашег третмана се даје у периоду од 90 минута и здравствени радник ће вас посматрати током примене у случају да се појави било која нуспојава. Ако се прва доза добро подноси, следеће дозе се могу давати у периоду од 30 минута (погледајте одељак 2 "Упозорења и мере предострожности"). Број инфузија које ћете примити зависиће од вашег одговора на лечење. Ваш лекар ће разговарај са њом о томе.
Код пацијената са раним раком дојке, метастатским раком дојке и метастатским раком желуца, Херцептин се примењује сваке 3 недеље. Херцептин се такође може давати једном недељно за лечење метастатског рака дојке.
Да бисте избегли грешке са лековима, важно је проверити налепнице на бочици како бисте били сигурни да је лек који се припрема и примењује Херцептин (трастузумаб), а не трастузумаб емтансин.
Предозирање Шта учинити ако сте узели превише Херцептина
Нема познатих ефеката који се могу приписати предозирању Херцептином.
Ако престанете да користите Херцептин
Немојте престати са узимањем овог лека без претходног разговора са лекаром. Све дозе треба узимати у право време сваке недеље или сваке три недеље (у зависности од вашег распореда дозирања). То помаже да лек делује најбоље.
Може проћи и до 7 месеци док се Херцептин не избаци из тела. Због тога ће ваш лекар можда одлучити да настави да прати вашу функцију срца чак и након завршетка лечења.
Ако имате додатних питања о употреби овог лека, питајте свог лекара, фармацеута или медицинску сестру
Нежељени ефекти Који су нежељени ефекти Херцептина
Као и сви други лијекови, Херцептин може изазвати нуспојаве, иако се оне неће јавити код свих. Неки од ових нежељених ефеката могу бити озбиљни и могу захтевати хоспитализацију.
Током инфузије Херцептина могу се јавити реакције као што су зимица, грозница и други симптоми слични грипу. Ови ефекти су врло чести (могу се јавити код више од 1 на 10 особа). Остали симптоми повезани са инфузијом су: мучнина, повраћање, бол, повећани мишићи напетост и дрхтавица, главобоља, вртоглавица, отежано дисање, пискање, висок или низак крвни притисак, поремећаји срчаног ритма (лупање срца, убрзан или неправилан рад срца), отицање лица или усана, осип на кожи и осећај умора. Неки од ових симптома могу бити тешки, а неки пацијенти су умрли (погледајте одељак 2 "Упозорења и мере предострожности").
Ови ефекти се углавном јављају при првој интравенозној инфузији ("капање" у вену) и током првих неколико сати након почетка инфузије. Они су углавном привремени. Здравствени радник ће вас надзирати током инфузије и најмање шест сати након почетка прве инфузије и два сата након почетка других инфузија. Ако осетите реакцију, инфузија ће се успорити или прекинути и можда ћете добити третман за сузбијање нежељених ефеката. Инфузија се може наставити након побољшања симптома.
Повремено, симптоми почињу више од шест сати након почетка инфузије. Ако вам се то догоди, одмах се обратите лекару. Понекад се симптоми могу побољшати, а касније се погоршати.
Остали нежељени ефекти могу се појавити у било које вријеме током лијечења Херцептином, не само у вези с инфузијом. Проблеми са срцем понекад се могу јавити током лијечења, а повремено и након завршетка лијечења, а могу бити и озбиљни. Они укључују слабљење крви. Срчани мишић који може довести до затајења срца, упале (отицање, црвенило, врућина и бол) слузокоже срца и поремећаја срчаног ритма. То може довести до симптома као што су:
- недостатак даха (чак и ноћу),
- кашаљ,
- задржавање течности (отицање) у ногама или рукама,
- лупање срца (убрзан или неправилан рад срца).
Ваш лекар ће редовно пратити ваше срце током лечења, али морате одмах рећи свом лекару ако приметите неки од горе наведених симптома.
Ако осетите било који од горе наведених симптома када сте завршили са лечењем Херцептином, требало би да се обратите лекару и обавестите га / је о свом претходном лечењу Херцептином.
Веома чести нежељени ефекти Херцептина (могу се јавити у више од 1 на 10 особа):
- инфекције
- пролив
- констипација
- опекотине у грудима (диспепсија)
- слабост
- осип по кожи
- бол у грудима
- бол у стомаку
- бол у зглобовима
- низак број црвених крвних зрнаца и белих крвних зрнаца (који помажу у борби против инфекција) понекад повезан са грозницом
- мишићни бол
- коњунктивитис
- прекомерно кидање
- крварење из носа
- цурење носа
- губитак косе
- тремор
- валунзи
- вртоглавица
- проблеми са ноктима
- губитак тежине
- губитак апетита
- немогућност спавања (несаница)
- Промењен укус
- Низак број тромбоцита
- Утрнулост или пецкање прстију на рукама и ногама
- Црвенило, оток или жуљеви у устима и / или грлу
- Бол, оток, црвенило или утрнулост шака и / или стопала
Чести нежељени ефекти Херцептина (могу се јавити у до 1 на 10 особа):
- алергијске реакције
- сува уста и кожа
- инфекције грла
- суве очи
- инфекције бешике и коже
- знојење
- Шиндре
- умор и малаксалост
- упала синуса
- био забринут
- запаљење панкреаса или јетре
- депресија
- поремећаји бубрега
- промене у размишљању
- повећан мишићни тонус или напетост (хипертонија)
- астма
- бол у рукама и / или ногама
- плућни поремећаји
- сврби осип
- бол у леђима
- поспаност
- Бол у врату
- модрице
- болови у костима
- хемороиди
- бубуљице
- сврбеж
- грчеви у ногама
Мање чести нежељени ефекти Херцептина могу се јавити у до 1 на 100 људи:
- глувоћа
- осип са пшеницом
Ретки нежељени ефекти Херцептина: могу се јавити у до 1 на 1000 људи:
- слабост
- жутица
- упала / ожиљци плућа
Остали нежељени ефекти који су забележени при употреби Херцептина: учесталост се не може проценити из доступних података:
- абнормалности или промене у згрушавању крви
- анафилактичке реакције
- висок ниво калијума
- отицање мозга
- отицање или крварење иза очију
- отицање срчане мембране
- успорен рад срца
- шок
- абнормални срчани ритам
- респираторни дистрес
- Респираторна инсуфицијенција
- акутно накупљање течности у плућима
- акутно сужавање дисајних путева
- абнормално смањење нивоа кисеоника у крви
- отицање грла
- отежано дисање у лежећем положају
- оштећење / отказивање јетре
- отицање лица, усана и грла
- отказивање бубрега ненормално смањење нивоа течности око бебе у материци
- неуспех развоја плућа у материци
- абнормални развој бубрега у материци
Неки од нежељених ефеката који се јављају могу бити последица рака дојке. Ако примате Херцептин у комбинацији са хемотерапијом, неки од ових нежељених ефеката такође могу бити последица хемотерапије.
Ако приметите било који од нежељених ефеката, обавестите свог лекара, фармацеута или медицинску сестру.
Пријављивање нежељених ефеката
Ако добијете било које нежељено дејство, разговарајте са својим лекаром, фармацеутом или медицинском сестром.Ово укључује све могуће нуспојаве које нису наведене у овом упутству. Такође можете пријавити нуспојаве директно путем националног система за пријављивање наведених у Додатку В. Нежељена дејства можете помоћи пружити више информација о безбедности овог лека.
Истек и задржавање
Чувајте овај лек ван погледа и дохвата деце.
Немојте користити овај лек након истека рока ваљаности наведеног на кутији и на бочици иза ознаке ЕКСП. Датум истека се односи на последњи дан тог месеца.
Чувати у фрижидеру (2 ° Ц - 8 ° Ц).
Раствор за инфузију треба користити одмах након разблаживања. Немојте користити Херцептин ако приметите било какве честице или промене боје пре примене.
Лекове не треба одлагати у отпадне воде или у кућни отпад. Питајте свог фармацеута како да баците лекове које више не користите. То ће помоћи заштити животне средине.
Састав и фармацеутски облик
Шта Херцептин садржи
- Активна супстанца је трастузумаб.Свака бочица садржи 150 мг трастузумаба који се мора растворити у 7,2 мл воде за ињекције, а добијени раствор садржи приближно 21 мг / мл трастузумаба.
- Помоћни састојци су Л-хистидин хидрохлорид, Л-хистидин, α дихидрат, α-трехалоза, полисорбат 20.
Како Херцептин изгледа и садржај паковања
Херцептин је прашак за концентрат за раствор за инфузију који се испоручује у стакленој бочици затвореној гуменим чепом који садржи 150 мг трастузумаба. Прашак је бела до светло жута лиофилизована куглица. Свако паковање садржи 1 бочицу праха.
Упутство о извору: АИФА (Италијанска агенција за лекове). Садржај објављен у јануару 2016. Присутне информације можда нису ажурне.
Да бисте имали приступ најновијој верзији, препоручљиво је да приступите веб страници АИФА (Италијанска агенција за лекове). Одрицање од одговорности и корисне информације.
01.0 НАЗИВ ЛИЈЕКА
ХЕРЦЕПТИН 150 МГ ПРАХ У КОНЦЕНТРАТУ ЗА РАСТВОР ЗА ИНФУЗИЈУ
02.0 КВАЛИТАТИВНИ И КВАНТИТАТИВНИ САСТАВ
Једна бочица садржи 150 мг трастузумаба, хуманизованог ИгГ1 моноклоналног антитела, произведеног ћелијском културом сисара (ћелије јајника кинеског хрчка) у суспензији, пречишћеном афинитетном хроматографијом и јонском изменом, са специфичним поступцима инактивације и уклањања вируса.
Реконституисани раствор Херцептин садржи 21 мг / мл трастузумаба.
За потпуну листу помоћних супстанци (погледајте одељак 6.1).
03.0 ФАРМАЦЕУТСКИ ОБЛИК
Прашак за концентрат за раствор за инфузију.
Бели до светло жути лиофилизовани прах.
04.0 КЛИНИЧКЕ ИНФОРМАЦИЈЕ
04.1 Терапијске индикације
Карцином дојке
Метастатски рак дојке
Херцептин је индикован за лечење одраслих пацијената са ХЕР2 позитивним метастатским раком дојке (МБЦ):
• као монотерапија за лечење пацијената који су примили најмање два режима хемотерапије за метастатску болест. Раније примењена хемотерапија мора да садржи најмање један антрациклин и један таксан, осим ако је пацијент неприкладан за такве третмане. Пацијенти са позитивним хормонским рецепторима такође нису успели да одговоре на хормонску терапију, осим ако је пацијент неприкладан за такве третмане.
• у комбинацији са паклитакселом за лечење пацијената који нису примили хемотерапију због метастатске болести и за које лечење антрациклинима није индицирано.
• у комбинацији са доцетакселом за лечење пацијената који нису примили хемотерапију због своје метастатске болести.
• у комбинацији са инхибитором ароматазе у лечењу пацијената у постменопаузи са МБЦ позитивним на хормонске рецепторе који претходно нису лечени трастузумабом.
Рак дојке у раној фази
Херцептин је индикован за лечење одраслих пацијената са ХЕР2 позитивним раним раком дојке (ЕБЦ):
• после операције, хемотерапије (неоадјувантне или адјувантне) и радиотерапије (ако постоји) (видети одељак 5.1)
• после адјувантне хемотерапије доксорубицином и циклофосфамидом, у комбинацији са паклитакселом или доцетакселом.
• у комбинацији са адјувантном хемотерапијом са доцетакселом и карбоплатином.
• у комбинацији са неоадјувантном хемотерапијом, праћено адјувантном терапијом Херцептином, код локално узнапредовале болести (укључујући инфламаторни облик) или код тумора пречника> 2 цм (видети одељке 4.4 и 5.1).
Херцептин треба користити само код пацијената са метастатским или раним стадијумом рака дојке чији тумори показују прекомерну експресију ХЕР2 или амплификацију гена ХЕР2 како је утврђено тачним и потврђеним тестом (видети одељке 4.4 и 5.1).
Метастатски рак желуца
Херцептин у комбинацији са капецитабином или 5-флуороурацилом и цисплатином је индикован за лечење одраслих пацијената са метастатским аденокарциномом желуца или гастроезофагеалног споја ХЕР2 позитивним који раније нису примали антиканцерогени лек за метастатску болест.
Херцептин треба давати само пацијентима са метастатским раком желуца (МГЦ) чији тумори имају прекомерну експресију ХЕР2, дефинисану као резултат ИХЦ2 + и потврђену резултатом СИСХ или ФИСХ, или дефинисану као резултат ИХЦ3 +. Морају се користити тачне и валидиране методе одређивања (видети одељке 4.4 и 5.1).
04.2 Дозирање и начин примене
Мерење експресије ХЕР2 је обавезно пре почетка терапије (видети одељке 4.4 и 5.1). Лечење Херцептином треба да започне само лекар са искуством у примени цитотоксичне хемотерапије (видети одељак 4.4) и треба да га примењује само здравствени радник .
Важно је проверити означавање лека како бисте били сигурни да се пацијенту даје тачна формулација (интравенозна или поткожна фиксна доза) како је прописано. Херцептин интравенозна формулација није намењена за поткожну примену и треба је примењивати само интравенозном инфузијом.
Прелазак са третмана са Херцептин интравенозном формулацијом на третман са Херцептин поткожним обликом и обрнуто, даван сваке три недеље (к3в), испитиван је у студији МО22982 (видети одељак 4.8).
Да бисте избегли грешке са лековима, важно је проверити налепнице на бочици како бисте били сигурни да је лек који припремате и дајете Херцептин (трастузумаб), а не Кадцила (трастузумаб емтансин).
Дозирање
Метастатски рак дојке
Администрација сваке три недеље
Препоручена почетна учитавајућа доза је 8 мг / кг телесне тежине.Препоручена доза одржавања у интервалима од три недеље је 6 мг / кг телесне тежине, почевши три недеље након пуњења.
Недељна администрација
Препоручена почетна учитавајућа доза Херцептина је 4 мг / кг телесне тежине. Препоручена недељна доза одржавања Херцептина је 2 мг / кг телесне тежине, почевши недељу дана након пуњења.
Примена у комбинацији са паклитакселом или доцетакселом
У кључним студијама (Х0648г, М77001), паклитаксел или доцетаксел су давани дан након прве дозе Херцептина (за дозу, погледајте Резиме карактеристика производа (СмПЦ) паклитаксела или доцетаксела) и одмах након следећих доза Херцептина ако је претходна Доза Херцептина се добро подносила.
Примена у комбинацији са инхибитором ароматазе
У кључној студији (БО16216) Херцептин и анастрозол су давани од првог дана. Није било ограничења у погледу времена примене Херцептина и анастрозола (за дозу видети СмПЦ за анастрозол или друге инхибиторе ароматазе).
Рак дојке у раној фази
Администрација сваке три недеље и недељно
Када се примењује три пута недељно, препоручена почетна учитавајућа доза Херцептина је 8 мг / кг телесне тежине. Препоручена доза одржавања Херцептина у интервалима од три недеље је 6 мг / кг телесне тежине, почевши три недеље након пуњења.
У недељној примени (почетна учитавајућа доза од 4 мг / кг, затим 2 мг / кг једном недељно), истовремено са паклитакселом након хемотерапије доксорубицином и циклофосфамидом.
Видети одељак 5.1 за дозу комбиноване хемотерапије.
Метастатски рак желуца
Администрација сваке три недеље
Препоручена почетна учитавајућа доза је 8 мг / кг телесне тежине. Препоручена доза одржавања у интервалима од три недеље је 6 мг / кг телесне тежине, почевши три недеље након пуњења.
Метастатски и рани стадијум рака дојке и метастатски рак желуца
Трајање лечења
Пацијенте са метастатским раком дојке или метастатским раком желуца треба лечити Херцептином до прогресије болести. Пацијенткиње са раним раком дојке треба да се лече Херцептином 1 годину или док се не појави рецидив, шта год пре наступи.Не препоручује се продужење лечења у ЕБЦ -у дуже од једне године (видети одељак 5.1).
Смањење дозе
У клиничким испитивањима није било смањења дозе Херцептина. Пацијенти могу наставити терапију леком Херцептин током периода реверзибилне мијелосупресије изазване хемотерапијом, али их у том периоду треба пажљиво пратити због компликација повезаних са неутропенијом. Погледајте СмПЦ пацлитакела, доцетаксела или инхибитора ароматазе да бисте смањили или одложили дозирање.
Ако се проценат избацивања фракције леве коморе (ЛВЕФ) смањи ≥ 10 бодова од почетне вредности и падне испод 50%, дозирање треба обуставити и поновити процену ЛВЕФ у року од приближно 3 недеље. Ако се ЛВЕФ не побољша или додатно смањи, или ако се развије симптоматска конгестивна срчана инсуфицијенција (ЦХФ), треба озбиљно размислити о прекиду примене Херцептина, осим ако користи за појединачног пацијента превазилазе ризике. Све ове пацијенте ће морати прегледати кардиолог и временом пратити.
Пропуштене дозе
Ако је пацијент пропустио дозу Херцептина недељу дана или мање, уобичајену дозу одржавања Херцептина (недељно: 2 мг / кг, сваке 3 недеље: 6 мг / кг) треба дати што је пре могуће. Не чекајте следећи заказани циклус. Накнадне дозе одржавања Херцептина треба применити 7 или 21 дан касније у зависности од режима дозирања: недељно или сваке три недеље.
Ако је пацијент пропустио дозу Херцептина дуже од једне недеље, нову пуну дозу Херцептина треба дати за приближно 90 минута (недељна примена: 4 мг / кг, примена сваке 3 недеље: 8 мг / кг) чим могуће. Накнадне дозе одржавања Херцептина (недељна примена: 2 мг / кг, примена сваке 3 недеље: 6 мг / кг, респективно) треба применити 7 или 21 дан касније у зависности од одговарајућег режима дозирања: недељно или сваке три недеље.
Посебне популације
Фармакокинетичке студије нису спроведене код старије популације и код особа са бубрежном или јетреном дисфункцијом. У популационој фармакокинетичкој анализи старост и бубрежно оштећење нису променили доступност трастузумаба.
Педијатријска популација
Нема индикација за специфичну употребу Херцептина у педијатријској популацији.
Начин примене
Оптерећујућу дозу Херцептина треба примијенити као 90 -минутну интравенску инфузију. Не примењивати као интравенозну ињекцију или интравенозни болус. Интравенску инфузију Херцептина треба да дају здравствени радници обучени за лечење анафилаксије и у присуству опреме за хитне случајеве. Пацијенте треба посматрати најмање шест сати након почетка прве инфузије и два сата након почетка наредних инфузија због симптома, попут грознице и зимице или других симптома повезаних са инфузијом (видети одељке 4.4 и 4.8. Ови симптоми могу контролише заустављањем инфузије или успоравањем брзине. Инфузија се може наставити када се симптоми ублаже.
Ако се почетна доза пуњења добро подноси, следеће дозе се могу применити као 30 -минутна инфузија.
За упутства о реконституцији Херцептин интравенозне формулације пре примене, погледајте одељак 6.6.
04.3 Контраиндикације
• Позната преосетљивост на трастузумаб, мишје протеине или било коју помоћну супстанцу наведену у одељку 6.1.
• Пацијенти са тешком диспнејом у мировању, услед компликација узнапредовалог малигнитета, или пацијенти којима је потребна додатна терапија кисеоником.
04.4 Посебна упозорења и одговарајуће мере опреза при употреби
Да би се побољшала следљивост биолошких лекова, комерцијални назив и број серије примењеног производа морају бити јасно забележени (или декларисани) у медицинском картону пацијента.
Тестирање на ХЕР2 мора се обавити у специјализованој лабораторији која може гарантовати одговарајућу валидацију аналитичких поступака (видети одељак 5.1).
Тренутно нема података из клиничких испитивања о поновном лечењу пацијената који су претходно били изложени Херцептину ради адјувантног лечења.
Срчана дисфункција
Опште разматрање
Пацијенти који се лече Херцептином имају повећан ризик од развоја ЦХФ (Класа ИИ-ИВ према Нев Иорк Хеарт Ассоциатион [НИХА]) или асимптоматска срчана дисфункција. Ови догађаји су примећени код пацијената који су лечени само Херцептином или у комбинованој терапији са паклитакселом или доцетакселом, нарочито након хемотерапије антрациклинима (доксорубицин или епирубицин). Умереног до тешког интензитета и повезани су са смрћу (видети одељак 4.8). Поред тога, треба бити посебно опрезан при лечењу пацијената са повећаним срчаним ризиком, нпр. хипертензија, потврђена болест коронарних артерија, ЦХФ, фракција избацивања леве коморе (ЛВЕФ) у старости.
Сви кандидати за лечење Херцептином, а посебно пацијенти који су претходно били изложени лечењу антрациклином и циклофосфамидом (АЦ), требало би да се подвргну основној процени срчаног статуса, укључујући историју и физички преглед, електрокардиограм (ЕКГ), ехокардиограм и / или скенирање вишеструких улаза (МУГА) или МРИ. Праћење може помоћи у идентификацији пацијената код којих се развије срчана дисфункција. Процену срчане функције, спроведену на начин почетне, треба поновити свака 3 месеца током лечења и сваких 6 месеци по прекиду лечења до 24 месеца након последње примене Херцептина.
На основу популационе фармакокинетичке анализе свих доступних података (видети одељак 5.2), трастузумаб може остати у циркулацији до 7 месеци након престанка примене Херцептина. Пацијенти који примају антрациклине након завршетка терапије Херцептином могу имати повећан ризик од срчане дисфункције. Ако је могуће, лекари треба да избегавају терапију антрациклинима до 7 месеци након престанка примене лека Херцептин.Уколико се користе антрациклини, треба пажљиво пратити срчану функцију пацијента.
Формалну кардиолошку процену треба размотрити код пацијената који су имали кардиолошке проблеме након почетног прегледа. Срчану функцију треба пратити током лечења код свих пацијената (нпр. Сваких 12 недеља). Праћење може помоћи у идентификацији пацијената код којих се развије срчана дисфункција. Пацијентима који развију асимптоматску срчану дисфункцију може бити од користи чешће праћење (нпр. Сваких 6-8 недеља). У случају пацијената који пријављују континуирано смањење функције леве коморе, али остају асимптоматски, лекар треба да размотри прекид терапије ако није примећена клиничка корист од терапије леком Херцептин.
Безбедност наставка или поновног почетка примене лека Херцептин код пацијената са срчаном дисфункцијом није испитивана у проспективним студијама. Ако се ЛВЕФ смањи за ≥ 10 поена у односу на почетну вредност и падне испод 50%, дозирање треба обуставити и поново проценити ЛВЕФ у року од приближно 3 недеље. Ако ЛВЕФ то учини ако се не побољша или даље опада, или се развије симптоматска ЦХФ, треба озбиљно размислити о прекиду примене Херцептина, осим ако се сматра да користи за појединачног пацијента превазилазе ризике Ове пацијенте треба да процени кардиолог и да их прати током времена.
Ако се током терапије Херцептином појави симптоматска срчана инсуфицијенција, треба је лечити стандардном терапијом лековима за ЦХФ. Већина пацијената који су развили ЦХФ или асимптоматску срчану дисфункцију у кључним студијама побољшали су се стандардним третманом са инхибитором ангиотензин конвертујућег ензима (АЦЕ) или блокатором ангиотензинских рецептора (АРБ) и бета блокатором Већина пацијената са срчаним симптомима и доказима клиничке користи повезане са Херцептином лечење је наставило терапију без даљих срчаних клиничких догађаја.
Метастатски рак дојке
Херцептин се не сме давати истовремено са антрациклинима у контексту МБЦ.
Пацијенти са МБЦ који су претходно примали антрациклине такође су у опасности од срчане дисфункције при лечењу Херцептином, иако је овај ризик мањи него код истовремене употребе Херцептина и антрациклина.
Рак дојке у раној фази
За пацијенте са ЕБЦ -ом, кардиолошку процену, спроведену на начин прве, треба поновити свака 3 месеца током лечења и сваких 6 месеци након престанка лечења, до 24 месеца након последње примене Херцептина. Препоручује се додатно праћење код пацијената који примају хемотерапију засновану на антрациклинима, која би се требала одвијати годишње до 5 година након последње примене Херцептина, или дуже ако се примети континуирано смањење ЛВЕФ-а.
Пацијенти са историјом инфаркта миокарда (МИ), ангином пекторис која захтева лечење, претходном или тренутном ЦХФ (НИХА класа ИИ-ИВ), кардиомиопатијом ЛВЕФ, срчаном аритмијом која захтева медицинско лечење, клинички значајном валвуларном болешћу срца, лошом контролом хипертензије (контролисана хипертензија одговарајућим стандардним медицинским третманом) и хемодинамски значајни перикардни излив искључени су из кључних студија адјувантног и неоадјувантног ЕБЦ третмана са Херцептином. Због тога се лечење не може препоручити код ових пацијената.
Помоћни третман
Херцептин се не сме примењивати истовремено са антрациклинима у контексту адјувантног лечења.
Повећана инциденца симптоматских и асимптоматских срчаних догађаја примећена је код пацијената са раним карциномом дојке када је Херцептин даван након хемотерапије засноване на антрациклинима у поређењу са давањем са доцетакселом и неантрациклин карбоплатином и био је израженији када се Херцептин примењивао истовремено са таксанима него када се узастопно дају таксанима. Без обзира на режим који се користи, већина симптоматских срчаних догађаја догодила се у првих 18 месеци. У једној од 3 кључне студије у којима је пратити средња вредност од 5,5 година (БЦИРГ006) примећено је стално повећање кумулативне стопе симптоматских срчаних догађаја или ЛВЕФ код пацијената који су примали Херцептин истовремено са таксаном након терапије антрациклинима до 2,37% у поређењу са приближно 1. 1% у два поређења оружје (антрациклин плус циклофосфамид праћен таксаном и таксаном, карбоплатином и Херцептином).
Четири велике студије спроведене у адјувантном окружењу идентификовале су срчане факторе ризика, укључујући: старију старост (> 50 година), низак ЛВЕФ (антихипертензивни лекови. Код пацијената лечених Херцептином након завршетка адјувантне хемотерапије, ризик од срчане дисфункције повезан је са већа кумулативна доза антрациклина дата пре почетка терапије Херцептином и индекс телесне масе (БМИ)> 25 кг / м2.
Неоадјувантно-адјувантни третман
Код пацијената са ЕБЦ-ом који су кандидати за неоадјувантно-адјувантно лечење, Херцептин треба примењивати истовремено са антрациклинима само код пацијената који нису примили хемотерапију и само са ниским дозама антрациклина, односно максималним кумулативним дозама доксорубицина 180 мг / м2 или епирубицина 360 мг / м2.
Ако су пацијенти истовремено лечени пуним циклусом малих доза антрациклина и Херцептина у неоадјувантном окружењу, не треба давати даљу цитотоксичну хемотерапију након операције. У другим ситуацијама, одлука о потреби додатне цитотоксичне хемотерапије мора се донети према индивидуалним факторима.
До сада је искуство истовремене примене трастузумаба са ниским дозама антрациклинских режима ограничено на две студије (МО16432 и БО22227).
У кључној студији МО16432, Херцептин је примењен истовремено са неоадјувантном хемотерапијом, која је садржавала три курса доксорубицина (кумулативна доза од 180 мг / м2).
Учесталост симптоматске срчане дисфункције била је 1,7% у краку који је садржавао Херцептин.
Кључна студија БО22227 је осмишљена да покаже неинфериорност третмана са поткожном формулацијом Херцептина у поређењу са интравенозном формулацијом Херцептина заснованом на ко-примарним крајњим тачкама ПК и ефикасности (Цт пре тразузумаба циклуса 8 пре дозе и стопа пЦР-а при дефинитивној операцији, респективно) (види Одељак 5.1 СмПЦ -а поткожне формулације Херцептин). У кључној студији БО22227, Херцептин је примењен истовремено са неоадјувантном хемотерапијом која је садржавала четири курса епирубицина (кумулативна доза од 300 мг / м2); при средњем праћењу од 40 месеци, учесталост конгестивне срчане инсуфицијенције била је 0,0% у интравенозној руци са Херцептином.
Клиничко искуство код пацијената старијих од 65 година је ограничено.
Реакције повезане са инфузијом и преосетљивост
Пријављене су озбиљне нежељене реакције повезане са инфузијом Херцептина, укључујући диспнеју, хипотензију, пискање, хипертензију, бронхоспазам, суправентрикуларну тахиаритмију, смањену засићеност кисеоником, анафилаксу, респираторни дистрес, уртикарију и ангиоедем (видети одељак 4.8). Премедикација се може користити за смањење ризика од таквих догађаја. Већина ових догађаја се јавља током или у року од 2,5 сата од почетка прве инфузије.Уколико дође до инфузионе реакције, инфузију Херцептина треба прекинути или успорити брзину инфузије и пратити пацијента док не нестану сви уочени симптоми (видети одељак 4.2 Ови симптоми се могу лечити аналгетицима / антипиретицима, као што су меперидин или парацетамол, или антихистаминицима као што је дифенхидрамин. Већина пацијената је искусила решавање симптома симптома, а затим су примили додатне инфузије Херцептина. Озбиљне реакције су успешно лечене са супортивна терапија, као што су кисеоник, бета агонисти и кортикостероиди. У ретким случајевима, ове реакције су биле повезане са клиничким током који је кулминирао смртоносним исходом. Пацијенти који доживе диспнеју у мировању, услед компликација узнапредовалих тумора и коморбидитета, могу бити под већим ризиком већа да доживи фаталну реакцију на инфузију. Због тога се ови пацијенти не смеју лечити Херцептином (видети одељак 4.3).
Пријављена су и почетна побољшања праћена клиничким погоршањем и одложене реакције са брзим клиничким погоршањем. Смрт се догодила у року од неколико сати до једне седмице након инфузије. У врло ријетким случајевима, пацијенти су доживјели почетак инфузијских реакција и плућне симптоме више од шест сати након почетка примјене Херцептина. Пацијенте их треба упозорити на могућност такве одложен почетак и треба их упутити да се обрате свом лекару ако се то догоди.
Плућни догађаји
У пост-маркетиншкој примени при примени Херцептина пријављени су тешки плућни догађаји (видети одељак 4.8). Ови догађаји су повремено били фатални. Пријављени су и случајеви интерстицијске болести плућа, укључујући плућне инфилтрате, синдром акутног респираторног дистреса, упалу плућа., Плућа упала, плеурални излив, респираторни дистрес, акутни плућни едем и респираторна инсуфицијенција Фактори ризика повезани са интерстицијалном плућном болешћу укључују претходну или истовремену терапију другим анти-неопластичним третманима као што су таксани, гемцитабин, винорелбин и радиотерапија, за које је таква повезаност већ позната Ови догађаји се могу јавити у контексту инфузионе реакције или имају одложен почетак. Пацијенти који доживе диспнеју у мировању, услед компликација узнапредовалих тумора и коморбидитета, могу бити у већем ризику од доживљавања догађаја. Ови пацијенти нти стога не треба лечити Херцептином (видети одељак 4.3). Потребан је опрез у присуству упале плућа, посебно код пацијената који се истовремено лече таксанима.
04.5 Интеракције са другим лековима и други облици интеракција
Нису спроведена формална испитивања интеракција лекова. У клиничким студијама нису примећене клинички значајне интеракције између Херцептина и лекова који се примењују истовремено.
Ефекат трастузумаба на фармакокинетику других антинеопластика
Фармакокинетички подаци из студија БО15935 и М77004 код жена са ХЕР2 позитивним метастатским раком дојке сугеришу да изложеност паклитакселу и доксорубицину (и њиховим главним метаболитима 6-α хидроксил-паклитакселу, ПОХ и доксорубицинол, ДОЛ) није промењена присуством трастузумаба (ИВ оптерећујућа доза 8 мг / кг или 4 м / кг након чега следи 6 мг / кг к3в или 2 мг / кг к1в ИВ, респективно).
Међутим, трастузумаб може повећати укупну изложеност метаболита доксорубицина (7-деокси-13 дихидро-доксорубицинон, Д7Д). Биоактивност Д7Д и клинички ефекат повећања овог метаболита нису били јасни.
Подаци из студије ЈП16003, у једној руци са Херцептином (ИВ учитавајућа доза 4 мг / кг и ИВ 2 мг / кг недељно) и доцетакселом (60 мг / м2 ИВ), спроведени код Јапанки са ХЕР2 позитивним метастатским раком дојке, сугеришу да истовремена примена примена Херцептина није имала утицаја на фармакокинетику доцетаксела у једној дози. ЈП19959 је подстудија студије БО18255 (ТоГА) спроведена код јапанских пацијената мушког и женског пола са узнапредовалим раком желуца ради проучавања фармакокинетичког профила капецитабина и цисплатина који су давани са или без Херцептина. Резултати ове подстудије указују на то да изложеност биоактивним метаболитима (нпр. 5-ФУ) капецитабина није промењена истовременом употребом монотерапије цисплатином или цисплатина са Херцептином. Међутим, сам капецитабин је показао веће концентрације и дужи полуживот у комбинацији са Херцептином. Подаци такође указују на то да се фармакокинетика цисплатина није променила истовременом применом капецитабина или капецитабина у комбинацији са Херцептином.
Фармакокинетички подаци из студије Х4613г / ГО01305 код пацијената са метастатским или локално узнапредовалим неоперабилним ХЕР2-позитивним карциномом дојке сугеришу да трастузумаб није утицао на фармакокинетику карбоплатина.
Ефекти антинеопластике на фармакокинетику трастузумаба
Поређењем симулираних серумских концентрација трастузумаба након монотерапије Херцептином (4 мг / кг оптерећујућа доза / 2 мг / кг к1в ИВ) и серумских концентрација примећених код Јапанки са ХЕР2 позитивним метастатским раком дојке (студија ЈП16003) показало је да истовремена примена доцетаксела није имала ефекта о фармакокинетици трастузумаба.
Поређење фармакокинетичких података из две студије ИИ фазе (БО15935 и М77004) и једне студије ИИИ фазе (Х0648г), у којој су пацијенти примали истовремени третман са Херцептином и паклитакселом, и две студије ИИ фазе у којима је Херцептин даван као монотерапија (В016229 и МО16982), код жена са ХЕР2 позитивним метастатским раком дојке, указује на то да појединачне и средње најниже концентрације трастузумаба у серуму варирају унутар и између студија, али није јасан утицај истовремене примене паклитаксела на фармакокинетику трастузумаба.Поређење фармакокинетичких података трастузумаба из студије М77004 у којој су жене са ХЕР2-позитивним метастатским раком дојке примале истовремени третман са Херцептином, паклитакселом и доксорубицином, и фармакокинетичким подацима трастузумаба у студијама у којима је Херцептин даван сам (Х0649г) или у комбинацији са антрациклином плус циклофосфамид или паклитаксел (студија Х0648г), сугерисали су да доксорубицин и паклитаксел немају утицаја на фармакокинетику трастузумаба.
Фармакокинетички подаци из студије Х4613г / ГО01305 сугеришу да карбоплатин нема утицаја на фармакокинетику трастузумаба.
Чини се да истовремена примена анастрозола није утицала на фармакокинетику трастузумаба.
04.6 Трудноћа и дојење
Жене у репродуктивном добу
Жене у репродуктивном периоду треба обавестити о потреби употребе ефикасне контрацепције током лечења Херцептином и 7 месеци по завршетку лечења (видети одељак 5.2).
Трудноћа
Студије репродукције су спроведене на мајмунима циномолгус у дозама до 25 пута веће од недељне људске дозе одржавања од 2 мг / кг Херцептин интравенозне формулације и није открило никакве доказе о смањеној плодности или оштећењу плода.Пренос трастузумаба плацентом је примећен током развојног периода. рани фетус (20-50. дана гестације ) и касно (120-150 дана трудноће). Није познато да ли Херцептин може утицати на репродуктивну способност. Пошто студије о репродукцији на животињама не предвиђају увек ефекте на „мушкарце, Херцептин треба избегавати у трудноћи, осим ако су потенцијалне користи за мајку надмашују потенцијалне ризике по фетус.
Након стављања лека у промет објављени су извештаји о оштећењу бубрежног развоја и / или функције у вези са олигохидрамнионом, неким повезаним са фаталном феталном плућном хипоплазијом, код трудница лечених Херцептином. У случају трудноће, жену треба обавестити о могућности оштећења фетуса. Помно праћење мултидисциплинарног тима пожељно је ако се трудница лечи Херцептином или ако дође до трудноће током лечења Херцептином или у року од 7 месеци након последње дозе лека.
Време храњења
Студија о мајмунима Циномолгус током лактације, у дозама 25 пута већим од недељне хумане дозе одржавања од 2 мг / кг Херцептин интравенозне формулације, показало се да се трастузумаб излучује у млеку. Присуство трастузумаба у серуму неонаталних мајмуна није било повезано са никаквим штетним ефектима на раст или развој од рођења до 1 месеца старости. Није познато да ли се трастузумаб излучује у мајчино млеко. Будући да се хумани ИгГ1 лучи у мајчино млеко и потенцијални ризик од оштећења новорођенчета није познат, жене не би требало да доје током терапије леком Херцептин и 7 месеци након последње дозе.
Плодност
Нема доступних података о плодности.
04.7 Утицај на способност управљања возилима и машинама
Херцептин нема или има занемарљив утицај на способност управљања возилима и рада на машинама. Међутим, пацијенте који развију симптоме повезане са инфузијом (видети одељак 4.4) треба саветовати да не возе и не рукују машинама док симптоми не нестану.
04.8 Нежељени ефекти
Сажетак сигурносног профила
Најозбиљније и / или уобичајене нежељене реакције пријављене до сада са применом Херцептина (интравенозна формулација и поткожна формулација) укључују: срчану дисфункцију, инфузионе реакције, хематотоксичност (нарочито неутропенију), инфекције и плућне нуспојаве.
Табеларна листа нежељених реакција
У овом одељку су коришћене следеће категорије учесталости: врло честе (≥1 / 10), честе (≥1 / 100,
Табела 1 приказује нежељене реакције које су пријављене при употреби интравенозног Херцептина самог или у комбинацији са хемотерапијом у кључним клиничким испитивањима иу постмаркетиншком окружењу.
Сви укључени изрази односе се на највећи проценат примећен у кључним клиничким студијама.
Табела 1: Нежељени ефекти пријављени код интравенозне примене Херцептина самих или у комбинацији са хемотерапијом у кључним клиничким испитивањима (Н = 8386) и у постмаркетиншком периоду
+ Указује на нежељене реакције пријављене у вези са фаталним исходом.
1 Указује на нежељене реакције пријављене углавном у вези са реакцијама везаним за инфузију. Нема специфичних процената за њих.
* Посматрано комбинованом терапијом након третмана антрациклинима, у комбинацији са таксанима.
Опис специфичних нежељених реакција
Срчана дисфункција
Конгестивна срчана инсуфицијенција (НИХА класа ИИ-ИВ) честа је нежељена реакција повезана са употребом Херцептина и повезана је са фаталним исходом (видети одељак 4.4). Знаци и симптоми срчане дисфункције, као што су диспнеја, ортопнеја, појачан кашаљ, плућни едем, с3 галоп, смањена фракција избацивања вентрикула, примећени су код пацијената лечених Херцептином (видети одељак 4.4).
У 3 кључна клиничка испитивања са Херцептином као помоћним средством у комбинацији са хемотерапијом, учесталост срчане дисфункције степена 3/4 (посебно симптоматска конгестивна срчана инсуфицијенција) била је слична код пацијената који су примали само хемотерапију (нпр. Они који нису примали Херцептин) и код пацијената који су примали Херцептин узастопно након таксана (0,3-0,4 %). Највећи проценат је примећен код пацијената који су примали Херцептин истовремено са таксаном (2,0 %). Искуство са истовременом применом Херцептина и ниским дозама антрациклинских режима у неоадјувантном окружењу је ограничено (види одељак 4.4).
Када је Херцептин даван након завршетка адјувантне хемотерапије, срчана инсуфицијенција НИХА класе ИИИ-ИВ примећена је код 0,6% пацијената у леченој руци током годину дана, након просечног праћења од 12 месеци. У студији БО16348, након просечног праћења од 8 година, учесталост тешке ЦХФ (НИХА класе ИИИ и ИВ) у једногодишњој групи са Херцептином била је 0,8%, а стопа дисфункције леве коморе била је благо симптоматска и асимптоматска 4,6% .
Озбиљна реверзибилност ЦХФ -а примећена је код 71,4% пацијената лечених Херцептином (дефинисано као низ од најмање две узастопне вредности ЛВЕФ ≥50% након догађаја). Реверзибилност је показана код 79,5% пацијената. Благо симптоматских и асимптоматских дисфункција леве коморе Приближно 17% догађаја повезаних са срчаном дисфункцијом догодило се након завршетка лечења Херцептином.
У кључним студијама о лечењу метастатске болести са Херцептин интравенозном формулацијом, учесталост срчане дисфункције варирала је између 9% и 12% када се лек примењивао у комбинацији са паклитакселом у поређењу са 1% - 4% само за паклитаксел. У монотерапији, стопа је била 6% - 9%. Највећа стопа срчане дисфункције догодила се код пацијената који су примали Херцептин истовремено са антрациклинима / циклофосфамидом (27%), и била је значајно већа него код само антрациклина / циклофосфамида (7% - 10%). У каснијој клиничкој студији са проспективним праћењем срчане функције, утврђено је да је учесталост симптоматске конгестивне срчане инсуфицијенције 2,2% код пацијената лечених Херцептином и доцетакселом у поређењу са 0% код пацијената који су лечени монотерапијом доцетакселом. Део пацијената (79% ) који су развили срчану дисфункцију у овим клиничким испитивањима побољшали су се након стандардног медицинског третмана за конгестивну срчану инсуфицијенцију.
Реакције на инфузију, реакције алергијског типа и преосетљивост
Процењује се да ће отприлике 40% пацијената лечених Херцептином доживети неки облик инфузионе реакције. Међутим, већина инфузионих реакција је благог до умереног интензитета (НЦИ-ЦТЦ систем бодовања) и имају тенденцију да се јаве у раној фази лечења, односно током једне инфузије , два и три, са мањом учесталошћу у наредним инфузијама. Такве реакције укључују зимицу, грозницу, диспнеју, хипотензију, пискање, бронхоспазам, тахикардију, смањену засићеност кисеоником, респираторни дистрес, осип, мучнину, повраћање и главобољу (видети одељак 4.4). у зависности од индикација, начина прикупљања података и примене трастузумаба истовремено са хемотерапијом или монотерапијом.
Тешке анафилактичке реакције које захтијевају хитне додатне интервенције обично се могу јавити током прве и друге инфузије Херцептина (видјети дио 4.4) и биле су повезане са фаталним исходом.
У изолованим случајевима примећене су анафилактоидне реакције.
Хематотоксичност
Фебрилна неутропенија и леукопенија су врло често уочени догађаји. Нежељене реакције које се обично развијају су: анемија, тромбоцитопенија и неутропенија. Учесталост епизода хипопротромбинемије није позната. Ризик од неутропеније може се незнатно повећати када се трастузумаб примјењује с доцетакселом након терапије антрациклинима.
Плућни догађаји
Озбиљне плућне нуспојаве јављају се заједно са употребом Херцептина и повезане су са фаталним исходом. То укључује, али се не ограничава на, плућне инфилтрате, синдром акутног респираторног дистреса, упалу плућа, упалу плућа, плеурални излив, респираторни дистрес, акутну плућну болест едем и респираторна инсуфицијенција (видети одељак 4.4).
Детаљи о мерама минимизирања ризика који су у складу са Европским планом управљања ризиком представљени су у Посебним упозорењима и мерама предострожности за употребу (одељак 4.4).
Имуногеност
У време неоадјувантно-адјувантног ЕБЦ третмана, 8,1% (24/296) пацијената лечених интравенозним Херцептином развило је антитела против трастузумаба (без обзира на присуство антитела на почетку). Неутрализирајућа антитијела на трастузумаб откривена су у узорцима након почетне фазе код 2 од 24 пацијента лијечена интравенозним Херцептином.
Клиничка важност ових антитела је непозната; међутим, чини се да ова антитела нису угрозила фармакокинетику, ефикасност (одређену комплетним патолошким одговором [пЦР]) и безбедност интравенозног Херцептина одређену појавом реакција повезаних са давањем (АРР).
Нема података о имуногености за Херцептин код рака желуца.
Прелазак са третмана са Херцептин интравенозном формулацијом на третман са Херцептин поткожним обликом и обрнуто
Студија МО22982 испитивала је прелаз са третмана са Херцептин интравенозном формулацијом на терапију са Херцептин поткожном формулацијом са примарним циљем процене склоности пацијената за интравенозну или поткожну примену трастузумаба. У испитивању су анализиране 2 кохорте (једна је третирана поткожном формулацијом у бочици, а друга поткожном формулацијом путем уређаја за испоруку) користећи двокраки укрштени дизајн, при чему је 488 пацијената рандомизовано у две различите секвенце третмана са Херцептином, датом сваком три недеље (ив [Циклуси 1-4] → сц [Циклуси 5-8] или сц [Циклуси 1-4] → ив [Циклуси 5-8]). Лекови који су били на терапији Херцептином ИВ (20,3%) или претходно изложени ИВ Херцептин (79,7%). За ИВ → сц секвенцу (комбиноване кохорте формулације поткожне бочице и формулације уређаја за поткожно давање) стопе повезане са нежељеним догађајима (свих степена) описане су пре преласка (циклуси 1-4) и након преласка (циклуси 5-8) као 53,8% наспрам 56,4%; за секвенцу сц → ев (комбиноване кохорте сцина бочица и с.ц. путем уређаја за испоруку), стопе нежељених догађаја (свих степена) описане су пре преласка и после пребацивања као 65,4% у односу на 48,7%.
Пре преласка (циклуси 1-4), стопе почетка озбиљних нежељених догађаја, нежељених догађаја 3. степена и прекид терапије због нежељених догађаја били су ниски (
Пријављивање сумње на нежељене реакције
Извештавање о сумњи на нежељене реакције које се јаве након добијања дозволе за лек важно је јер омогућава континуирано праћење односа користи и ризика лека. Од здравствених радника се тражи да пријаве све сумње на нежељене реакције путем националног система за пријављивање. "Адреса ввв. агензиафармацо.гов.ит/ит/респонсабили.
04.9 Предозирање
У клиничким студијама на људима нису забележени случајеви предозирања.У клиничким студијама нису примењиване појединачне дозе Херцептина, веће од 10 мг / кг. До овог нивоа, дозе су се добро подносиле.
05.0 ФАРМАКОЛОШКА СВОЈСТВА
05.1 Фармакодинамичка својства
Фармакотерапијска група: Антинеопластични агенси, моноклонска антитела, АТЦ ознака: Л01КСЦ03
Трастузумаб је рекомбинантно хуманизовано моноклонско антитело ИгГ1 против рецептора 2 хуманог епителног фактора раста (ХЕР2). Прекомерна експресија ХЕР2 примећена је код 20% -30% примарних карцинома дојке Студије о стопама позитивности ХЕР2 код карцинома желуца (ГЦ) откривене имунохистохемијом (ИХЦ) и хибридизацијом ин ситу флуоресцентна (ФИСХ) или хибридизација ин ситу хромогени (ЦИСХ) су показали да постоји "велика варијабилност у позитивности ХЕР2 у распону од 6,8% до 34,0% за ИХЦ и 7,1% до 42,6% за ФИСХ." Студије су показале да пацијенткиње са раком дојке са прекомерном експресијом ХЕР2 имају краће преживљавање без болести од пацијената са раком без прекомерне експресије ХЕР2. Изванстанични домен рецептора (ЕЦД, п105) може се отпустити у крвоток и мерити у узорцима серума.
Механизам дејства
Трастузумаб се "са високим афинитетом и специфичношћу везује за поддомен ИВ, перимембрански регион екстрацелуларног домена ХЕР2. Везивање трастузумаба за ХЕР2 инхибира сигнално независну сигнализацију ХЕР2 и спречава протеолитичко цепање његовог ванћелијског домена, механизам активације ХЕР2 Сходно томе, трастузумаб је показао обоје ин витро то код животиња, да би могло да инхибира пролиферацију ћелија туморског тумора које прекомерно експримирају ХЕР2. Ин витро Показало се да се АДЦЦ посредован трастузумабом првенствено врши на туморске ћелије са прекомерном експресијом ХЕР2 над туморским ћелијама које не прекомерно експримирају ХЕР2.
Детекција прекомерне експресије ХЕР2 или амплификације гена ХЕР2
Откривање прекомерне експресије ХЕР2 или појачања гена ХЕР2 код рака дојке
Херцептин треба користити само код пацијената са раком са прекомерном експресијом ХЕР2 или амплификацијом гена ХЕР2 како је утврђено тачним и потврђеним тестом. Прекомерна експресија ХЕР2 мора се открити имунохистохемијским (ИХЦ) прегледом фиксираних пресека тумора (видети одељак 4.4). Појачање гена ХЕР2 мора се открити хибридизацијом ин ситу флуоресценцијом (ФИСХ) или хибридизацијом ин ситу хромогени (ЦИСХ) фиксираних пресека тумора.Пацијенти код којих је изражена прекомерна експресија ХЕР2 са назнаком ИХЦ скора 3+ или позитивног ФИСХ или ЦИСХ резултата кандидати су за лечење Херцептином.
Да би се осигурали тачни и поновљиви резултати, испитивања се морају извести у специјализованим лабораторијама које могу гарантовати валидацију аналитичких поступака.
Препоручени систем за бодовање ИХЦ модела означавања је приказан у Табели 2:
Табела 2 Препоручени систем за бодовање ИХЦ образаца означавања за рак дојке
Генерално, ФИСХ тест се сматра позитивним ако је однос броја копија гена ХЕР2 по туморској ћелији према броју копија хромозома 17 већи или једнак 2 или ако постоји више од 4 копије ХЕР2 ген за туморске ћелије ако се хромозом 17 не користи као референца.
Генерално, ЦИСХ тест се сматра позитивним ако постоји више од 5 копија гена ХЕР2 по језгру у више од 50% ћелија рака.
За потпуна упутства о извођењу и тумачењу тестова погледајте летке приложене уз валидиране тестне пакете ФИСХ и ЦИСХ. Такође се могу применити званичне препоруке о тестирању ХЕР2.
За било коју другу методу која се може користити за процену експресије протеина или гена ХЕР2, анализе би требало да спроводе само лабораторије које обезбеђују оптималне перформансе валидираних метода. Такве методе морају бити јасне, прецизне и довољно тачне да покажу прекомерну експресију ХЕР2 и морају бити у стању да разликују умерену (ниво 2+) од високе (ниво 3+) прекомерну експресију ХЕР2.
Детекција прекомерне експресије ХЕР2 или појачања гена ХЕР2 код рака желуца
Само тачан и потврђен тест треба користити за одређивање прекомерне експресије или амплификације ХЕР2 гена. ИХЦ се препоручује као први тест и, у случајевима када је такође потребна процена амплификације гена ХЕР2, треба користити ин ситу хибридизацију јона сребра (СИСХ) или ФИСХ технику. Међутим, препоручује се СИСХ технологија која омогућава паралелну процену хистологије и морфологије тумора. Да би се обезбедила валидација процедура оцењивања и произвели тачни и поновљиви резултати, ХЕР2 тест мора да се изведе у лабораторији са обученим особљем. Потпуна упутства о извођењу теста и тумачењу резултата налазе се у информативном листу о производу који садржи тестове који се користе за вредновање ХЕР2.
У ТоГА студији (БО18255), пацијенти чији су тумори били ИХЦ3 + или ФИСХ позитивни дефинисани су као ХЕР2-позитивни и стога су укључени у студију. На основу резултата клиничких студија, позитивни ефекти били су ограничени на пацијенте са вишим нивоом прекомерне експресије протеина ХЕР2, дефинисане као 3+ са ИХЦ или 2+ са ИХЦ и позитиван резултат ФИСХ.
У студији поређења методологије (студија Д008548) примећен је висок степен слагања (> 95%) између техника СИСХ и ФИСХ за одређивање амплификације гена ХЕР2 код пацијената са раком желуца.
Прекомерна експресија ХЕР2 мора се одредити имунохистохемијским (ИХЦ) прегледом фиксираних пресека тумора.Појачање гена ХЕР2 мора се открити хибридизацијом ин ситу, користећи СИСХ или ФИСХ, на фиксним пресецима тумора.
Препоручени систем за бодовање ИХЦ модела означавања је приказан у Табели 3:
Табела 3 Препоручени систем за бодовање ИХЦ образаца означавања код рака желуца
Генерално, СИСХ или ФИСХ тестови се сматрају позитивним ако је однос броја копија гена ХЕР2 по ћелији тумора према броју копија хромозома 17 већи или једнак 2.
Клиничка ефикасност и безбедност
Метастатски рак дојке
Херцептин се самостално користио у клиничким испитивањима код пацијената са МБЦ са туморима које карактерише прекомерна експресија ХЕР2 и неуспех једног или више претходних режима хемотерапије за метастатску болест (само Херцептин).
Херцептин се такође користио у комбинацији са паклитакселом или доцетакселом за лечење пацијената који нису били хемотерапије због метастатске болести. Пацијенти који су претходно били лечени адјувантном хемотерапијом заснованом на антрациклинима лечени су паклитакселом (175 мг / м2 примењеним као 3-часовна инфузија) са или без Херцептина. У кључној студији са доцетакселом (100 мг / м2 у облику инфузије од 1 сата) са или без Херцептина, 60% пацијената је претходно примало адјувантну хемотерапију засновану на антрациклинима. Пацијенти су лечени Херцептином до прогресије болести.
Ефикасност Херцептина у комбинацији са паклитакселом код пацијената који претходно нису примали адјувантну терапију антрациклинима није проучавана.Међутим, комбинација Херцептина и доцетаксела је била ефикасна, без обзира на то да ли су пацијенти претходно примали адјувантну терапију или нису. Са антрациклинима.
Метода која се користи за анализу прекомерне експресије ХЕР2 и утврђивање подобности пацијената за учешће у кључним клиничким испитивањима монотерапије Херцептином и Херцептином плус паклитакселом користила је ХЕР2 имунохистохемијско бојење фиксираног материјала из тумора дојке, користећи мишја моноклонска антитела ЦБ11 и 4Д5. Ова ткива су фиксирана у формалину или Боуин -ов фиксатор. Ова метода испитивања која се користила у клиничким студијама и изведена у централној лабораторији користила је скалу од 0 до 3+. Укључени су пацијенти класификовани са 2+ или 3+ бојењем, док су они са 0 или 1+ бојењем искључени Више од 70% уписаних пацијената имало је 3+ „прекомерну експресију“. Добијени подаци указују на то да су корисни ефекти били већи код пацијената са вишим нивоима прекомерне експресије ХЕР2 (3+).
Примарна метода испитивања која се користила за одређивање ХЕР2 позитивности у кључној студији са доцетакселом, са или без Херцептина, била је имунохистохемија, а мањи број пацијената је тестиран хибридизацијом. ин ситу у флуоресценцији (ФИСХ). У овој студији, 87% укључених пацијената карактерише ИХЦ3 + болест, а 95% ИХЦ3 + и / или ФИСХ-позитивна болест.
Недељна примена код метастатског рака дојке
Резултати ефикасности монотерапије и комбинованих студија сажети су у Табели 4:
Табела 4 Резултати ефикасности из студија монотерапије и комбиноване терапије
ТТП = време до прогресије; "н.а." указује да се није могло оценити или да још није постигнуто.
1 Студија Х0649г: ИХЦ3 + субпопулације пацијената
2 Студија Х0648г: Субпопулације пацијената са ИХЦ3 +
3 Студија М77001: Популација намера да се лечи, резултати након 24 месеца
Комбиновано лечење Херцептином са анастрозолом
Херцептин је проучаван у комбинацији са анастрозолом за прву линију лечења пацијената у постменопаузи са ХЕР2 позитивним на хормонске рецепторе са прекомерно експресивном МБЦ (нпр. Рецептор естрогена (ЕР) и / или рецептор прогестерона (ПР)). Преживљавање без прогресије удвостручило се у Херцептину у комбинацији са групом анастрозола у поређењу са групом само са анастрозолом (4,8 месеци у односу на 2,4 месеца). За остале параметре, побољшања која су примећена у комбинованој групи била су: укупан одговор (16,5% наспрам 6,7%), клиничка корист (42,7% наспрам 27,9%), време до прогресије (4, 8 месеци у односу на 2,4 месеца). Није било разлике између две групе у погледу времена до одговора и трајања одговора. Просечно укупно преживљавање продужено је за 4,6 месеци за пацијенте у комбинованој групи. Разлика није била статистички значајна, међутим више од половине пацијената укључених у само групу анастрозола лечено је режимом који садржи Херцептин након прогресије болести.
Примена сваке три недеље код метастатског рака дојке
Подаци о ефикасности из упоредних студија монотерапије и комбиноване терапије сажети су у доњој Табели 5:
Табела 5 Резултати ефикасности из упоредних студија спроведених у монотерапији и у комбинованој терапији
ТТП = време до прогресије; "н.а." указује да се није могло оценити или да још није постигнуто.
1. Студија ВО16229: 8 мг / кг оптерећујућа доза, затим 6 мг / кг сваке 3 недеље
2. Студија МО16982: оптерећујућа доза 6 мг / кг недељно 3 пута; затим 6 мг / кг сваке 3 недеље
3. Студија БО15935
4. Студија МО16419
Прогрессион ситес
Стопа прогресије јетре значајно је смањена код пацијената лечених комбинацијом Херцептин-паклитаксел у поређењу са самим паклитакселом (21,8% наспрам 45,7%; п = 0,004). Више пацијената лечених Херцептином и паклитакселом показало је прогресију централног нервног система у поређењу са пацијентима леченим само паклитаксел (12,6% наспрам 6,5%; п = 0,377).
Рани стадијум рака дојке (адјувантна поставка)
Рак дојке у раној фази је дефинисан као инвазивни, неметастатски примарни рак дојке.
Употреба Херцептина у контексту адјувантне терапије испитивана је у 4 велике, мултицентричне, рандомизиране студије:
• Студија БО16348 је осмишљена за упоређивање третмана са Херцептином сваке три недеље током једне и две године у односу на посматрање само код пацијената са ХЕР2 позитивном ЕБЦ после операције, стандардне хемотерапије и радиотерапије (ако постоји). Такође је направљено поређење између лечења Херцептином једне године и лечења Херцептином две године. Пацијентима који су намеравали да приме Херцептин дата је почетна учитавајућа доза од 8 мг / кг, затим 6 мг / кг сваке три недеље током једне године или две године.
• Студије НСАПБ Б-31 и НЦЦТГ Н9831, укључујући обједињену анализу, осмишљене су за процену клиничке корисности комбиновања третмана Херцептином са паклитакселом након АЦ хемотерапије; поред тога, студија НЦЦТГ Н9831 је такође процењивала секвенцијално додавање Херцептина у односу на АЦ → П хемотерапију код пацијената са ХЕР2 позитивном ЕБЦ после операције.
• Студија БЦИРГ 006 је осмишљена да процени повезаност третмана Херцептином са доцетакселом након АЦ хемотерапије или доцетаксела и карбоплатина код пацијената са ХЕР2 позитивном ЕБЦ након операције.
Почетни карцином дојке у студији ХЕРА био је ограничен на операбилан, примарни, инвазивни аденокарцином дојке са позитивним аксиларним лимфним чворовима или негативним аксиларним лимфним чворовима, ако има тумор пречника најмање 1 цм.
У обједињеној анализи НСАПБ Б-31 и НЦЦТГ Н9831, ЕБЦ је био ограничен на жене са операбилним раком дојке високог ризика, дефинисаним као ХЕР2 позитивни и позитивни аксиларни лимфни чворови или ХЕР2 позитивни и аксиларни лимфни чворови негативни са карактеристикама високог ризика (величина тумора > 1 цм и ЕР негативан или величина тумора> 2 цм, без обзира на хормонски статус).
У студији БЦИРГ 006, ХЕР2 позитивна ЕБЦ била је ограничена на чворове позитивне или на чворове негативне пацијенте са високим ризиком дефинисане као одсуство захваћености лимфних чворова (пН0) и најмање 1 од следећег: величина тумора већа од 2 цм, естрогенски рецептори и прогестерон негативан, хистолошки и / или нуклеарни степен 2-3 или старији
Табела 6 резимира резултате ефикасности из студије БО16348 након медијалног праћења од 12 месеци *и 8 година **:
Табела 6 Резултати ефикасности из студије БО16348
* Једногодишња примарна крајња тачка ДФС-а у односу на посматрање достигла је задану статистичку границу
** Коначна анализа (укључујући укрштање 52% пацијената са посматрачке руке на Херцептин)
*** Постоји укупна разлика у узорку због малог броја пацијената који су рандомизирани након граничног датума за 12-мјесечну средњу анализу праћења
Резултати привремене анализе ефикасности премашили су унапред утврђену статистичку границу протокола за поређење Херцептина током 1 године са посматрањем. Након медијане праћења од 12 месеци, однос ризика (ХР) за преживљавање без болести (ДФС) био је 0,54 (95% ЦИ 0,44-0,67) што представља апсолутну корист, у смислу двогодишње стопе преживљавања без болести, од 7,6 процентних поена (85, 8% наспрам 78,2%) у корист групе са Херцептином.
Након просечног праћења од 8 година, извршена је коначна анализа која је открила да је лечење Херцептином током једне године било повезано са смањењем ризика за 24% у односу на само посматрање (ХР = 0,76, ЦИ на 95% 0,67 - 0,86) Ово представља апсолутну корист у смислу осмогодишње стопе преживљавања без прогресије болести од 6,4 процентних поена у корист терапије Херцептином током једне године.
У овој коначној анализи, продужење терапије Херцептином за две године није показало никакву додатну корист у односу на лечење за годину дана [ХР ДФС у двогодишњој у односу на једногодишњу популацију намере за лечење (ИТТ) = 0,99 (95% ЦИ: 0,87 - 1,13), п -вредност = 0,90 и ХР ОС = 0,98 (0,83 - 1,15); п -вредност = 0,78] Стопа асимптоматске дисфункције леве коморе повећана је у групи за лечење 2 године (8,1% наспрам 4,6% у више пацијената имало је најмање један нежељени догађај степена 3 или 4 у двогодишњој групи лечења (20,4%) у односу на годину дана лечења (16,3%).
У студијама НСАПБ Б-31 и НЦЦТГ Н9831, Херцептин је даван у комбинацији са паклитакселом, после АЦ хемотерапије.
Доксорубицин и циклофосфамид су истовремено давани на следећи начин:
• интравенски потисни доксорубицин, 60 мг / м2, даван сваке 3 недеље током 4 циклуса.
• интравенозни циклофосфамид, 600 мг / м2 током 30 минута, примењен сваке 3 недеље током 4 циклуса
Пацлитакел, у комбинацији са Херцептином, примењиван је на следећи начин:
• интравенски паклитаксел - 80 мг / м2 као континуирана интравенска инфузија, која се даје једном недељно током 12 недеља,
или
• интравенски паклитаксел - 175 мг / м2 у облику континуиране интравенске инфузије, примењује се једном у 3 недеље током 4 циклуса (1. дан сваког циклуса).
Резултати ефикасности из обједињене анализе НСАПБ Б-31 и НЦЦТГ 9831 у време коначне анализе ДФС * сумирани су у Табели 7. Просечно трајање праћења било је 1,8 година за пацијенте у АЦ групи → П и 2,0 године за пацијенте у руци АЦ → ПХ.
Табела 7 Резиме резултата ефикасности из обједињене анализе НСАБП Б-31 и НЦЦТГ 9831 у време коначне анализе ДФС *
А: доксорубицин; Ц: циклофосфамид; П: паклитаксел; Х: трастузумаб
* При средњем трајању праћења од 1,8 година за пацијенте у групи АЦ → П и 2,0 године за пацијенте у групи АЦ → ПХ.
** П-вредност за ОС није прешла унапред утврђену статистичку границу за поређење АЦ → ПХ у односу на АЦ → П.
У односу на "крајња тачка примарни, ДФС, додавањем Херцептина хемотерапији паклитакселом резултирало је смањењем ризика од понављања болести за 52%. Однос опасности се претвара у апсолутну корист, у смислу стопе преживљавања без болести у 3 године од 11,8% (87,2% наспрам 75,4 %) у корист АЦ → ПХ (Херцептин) крака.
У време ажурирања безбедности, након просечног праћења од 3,5-3,8 година, „анализа ДФС-а је поново потврдила обим користи приказане у коначној анализи ДФС-а. укрштање Херцептина у контролној групи, додавање Херцептина хемотерапији паклитакселом резултирало је смањењем ризика од понављања болести за 52% .Додавање Херцептина хемотерапији паклитакселом такође је резултирало смањењем рецидива болести за 37%.
Коначна унапред планирана анализа ОС из комбиноване анализе студија НСАБП Б-31 и НЦЦТГ 9831 спроведена је у време 707 смрти (медијан праћења 8,3 године у групи АЦ → ПХ). У поређењу са оним примећеним код АЦ → П третмана, АЦ → ПХ третман је резултирао статистички значајним побољшањем ОС (стратификовани ХР = 0,64; 95% ЦИ [0,55-0,74]; п-вредност лог-ранк
Коначни резултати ОС из збирне анализе НСАБП Б-31 и НЦЦТГ 9831 сумирани су у доњој Табели 8.
Табела 8 Коначна анализа укупног преживљавања из комбиноване анализе НСАБП Б-31 и НЦЦТГ 9831
А: доксорубицин; Ц: циклофосфамид; П: паклитаксел; Х: трастузумаб
ДФС анализа је такође спроведена у коначној анализи ОС која је произашла из комбиноване анализе НСАБП Б -31 и НЦЦТГ Н9831. Ажурирани резултати ДФС анализе (стратификовани ХР = 0,61; 95% ЦИ [0,54 - 0,69]) показали су Корист од ДФС -а је слична оној која је уочена у дефинитивној примарној анализи ДФС -а, упркос 24,8% пацијената у преласку АЦ → П руке на лечење Херцептином. Стопа преживљавања без болести од 77,2% (95% ЦИ: 75,4% - 79,1% ) у групи АЦ → ПХ процењена је на 8 година, са апсолутном користи од 11,8% у поређењу са групом АЦ → П.
У студији БЦИРГ 006 Херцептин је даван у комбинацији са доцетакселом, након хемотерапије са АЦ (АЦ → ДХ) или у комбинацији са доцетакселом и карбоплатином (ДЦарбХ).
Доцетаксел је даван на следећи начин:
• интравенски доцетаксел - 100 мг / м2 у облику једночасовне интравенске инфузије која се даје сваке 3 недеље током 4 циклуса (2. дан првог циклуса доцетаксела, затим 1. дан сваког следећег циклуса)
или
• интравенски доцетаксел - 75 мг / м2 у облику једночасовне интравенске инфузије, која се даје сваке 3 недеље током 6 циклуса (2. дан првог циклуса, затим 1. дан сваког следећег циклуса)
затим:
• карбоплатин - при циљаној АУЦ = 6 мг / мл / мин који се даје као интравенозна инфузија у трајању од 30-60 минута, понавља се сваке 3 недеље, укупно шест циклуса
Херцептин се давао једном недељно у комбинацији са хемотерапијом, а затим свака 3 недеље укупно 52 недеље.
Резултати ефикасности БЦИРГ 006 сумирани су у Табелама 9 и 10. Средње трајање праћења је било 2,9 година у групи АЦ → Д и 3,0 године у свакој од група АЦ → ДХ и ДЦарбХ.
Табела 9 Сажетак анализа ефикасности из студије БЦИРГ 006 АЦ → Д наспрам АЦ → ДХ
АЦ → Д = доксорубицин у комбинацији са циклофосфамидом, затим доцетаксел; АЦ → ДХ = доксорубицин у комбинацији са циклофосфамидом, затим доцетаксел у комбинацији са трастузумабом; ЦИ = интервал поверења.
Табела 10 Сажетак анализа ефикасности из студије БЦИРГ 006 АЦ → Д наспрам ДЦарбХ
АЦ → Д = доксорубицин у комбинацији са циклофосфамидом, затим доцетаксел; ДЦарбХ = доцетаксел, карбоплатин и трастузумаб; ЦИ = интервал поверења
У студији БЦИРГ 006 у вези са "крајња тачка примарни, ДФС, однос опасности се преводи у апсолутну корист, у смислу трогодишњег преживљавања без болести, од 5,8 процентних поена (86,7% наспрам 80,9%) у корист АЦ → ДХ групе (Херцептин) и 4,6 процентних поена (85,5% наспрам 80,9%) у корист руке ДЦарбХ (Херцептин) у односу на АЦ → Д.
У студији БЦИРГ 006, 213/1075 пацијената у групи ДЦарбХ (ТЦХ), 221/1074 пацијената у групи са АЦ ДХ (АЦ ТХ) и 217/1073 у групи АЦ → Д (АЦ Т) имали су Карнофски статус перформанси ≤ 90 (80 или 90). У овој подгрупи пацијената није примећена корист од преживљавања без болести (ДФС) (однос ризика = 1,16; 95% ЦИ [0,73, 1,83] за ДЦарбХ (ТЦХ) у односу на АЦ групу. Д (АЦ Т); однос опасности 0,97; 95% ЦИ [0,60, 1,55] за АЦ ДХ (АЦ ТХ) наспрам АЦ Д крака).
Осим тога, урађена је и анализа пост-хоц експлоративни подаци из заједничке анализе (ЈА) НСАБП Б-31 / НЦЦТГ Н9831 и клиничке студије БЦИРГ006, комбинујући ДФС и симптоматске срчане догађаје, сажето у Табели 11:
Табела 11 Анализа пост-хоц истраживање резултата заједничке анализе (ЈА) НСАБП Б-31 / НЦЦТГ Н9831 и клиничке студије БЦИРГ006, комбинујући ДФС и симптоматске срчане догађаје
О: доксуробицин; Ц: циклофосфамид; П: паклитаксел; Д: доцетаксел; Угљени хидрати: карбоплатин; Х: трастузумаб
ЦИ = интервал поверења
* У време коначне анализе ДФС-а. Медијан трајања праћења био је 1,8 година у групи АЦ → П и 2,0 године у групи АЦ → ПХ.
Рак дојке у раној фази (неоадјувантно-адјувантни контекст)
До данас нема доступних резултата који упоређују ефикасност примењеног Херцептина са хемотерапијом у адјувантном окружењу са неоадјувантним / адјувантним окружењем.
У контексту неоадјувантно-адјувантног лечења, студија МО16432, мултицентрично, рандомизовано клиничко испитивање, осмишљена је да процени клиничку ефикасност истовремене примене Херцептина са неоадјувантном хемотерапијом која садржи и антрациклин и таксан, након чега следи Херцептин као помоћно средство. на укупно 1 годину лечења. Студија је обухватила пацијенте са новооткривеном локално узнапредовалом (фаза ИИИ) или упалном ЕБЦ. Пацијенти са туморима ХЕР2 + били су рандомизирани да примају неоадјувантну хемотерапију истовремено са неоадјувантно-адјувантним Херцептином или само неоадјувантном хемотерапијом.
У студији МО16432, Херцептин (учитавајућа доза од 8 мг / кг, праћена са 6 мг / кг у одржавању сваке 3 недеље) примењиван је истовремено са 10 курсева неоадјувантне хемотерапије на следећи начин:
• доксорубицин 60 мг / м2 и паклитаксел 150 мг / м2, примењене сваке 3 недеље током 3 циклуса,
затим
• Пацлитакел 175 мг / м2 примењен сваке 3 недеље током 4 циклуса,
затим
• ЦМФ 1. и 8. дан сваке 4 недеље током 3 циклуса,
након операције следи
• додатни курсеви адјувантног Херцептина (након завршетка 1 године терапије).
Резултати ефикасности из студије МО16432 сумирани су у Табели 12. Средње трајање праћења у групи са Херцептином било је 3,8 година.
Табела 12 Резултати ефикасности из студије МО16432
* дефинисано као одсуство инвазивног карцинома у дојци и аксиларним лимфним чворовима
Процењена је апсолутна корист од 13 процентних поена у корист групе Херцептин у погледу трогодишње стопе преживљавања без догађаја (65% наспрам 52%).
Метастатски рак желуца
Херцептин је проучаван у рандомизираној, отвореној, фази ИИИ ТоГА студији (БО18255) у комбинацији са хемотерапијом наспрам само хемотерапије.
Хемотерапија се спроводи на следећи начин:
• капецитабин - 1000 мг / м2 орално два пута дневно током 14 дана сваке 3 недеље током 6 циклуса (увече првог дана до јутра 15. дана сваког циклуса)
или
• Интравенски 5 -флуороурацил - 800 мг / м2 / дан као континуирана интравенска инфузија током 5 дана, која се даје сваке 3 недеље током 6 циклуса (од 1 до 5 дана сваког циклуса)
Сваки од два лека примењен је са:
• цисплатин - 80 мг / м2 сваке 3 недеље током 6 циклуса, дат 1. дана сваког циклуса.
Резултати ефикасности из студије БО18225 сумирани су у Табели 13:
Табела 13 Резултати ефикасности из студије БО18225
ФП + Х: Флуоропиримидин / цисплатин + Херцептин
ФП: флуоропиримидин / цисплатин
а Оддс ратио
У студију су укључени пацијенти који претходно нису били лечени због локално узнапредовалог или рецидива и / или метастатски неоперабилног ХЕР2 позитивног аденокарцинома желуца или гастроезофагеалног споја, а нису кандидати за куративни третман. Л "крајња тачка примарно је било укупно преживљавање, дефинисано као време од датума рандомизације до датума смрти из било ког узрока. У време анализе, укупно је умрло 349 рандомизованих пацијената: 182 пацијента (62,8%) у контролној групи и 167 пацијената (56,8%) у групи која је била у вези са подложним тумором.
Пост-хоц анализа подгрупе показује да су позитивни ефекти лечења ограничени на туморе са вишим нивоом протеина ХЕР2 (ИХЦ 2 + / ФИСХ + или ИХЦ 3+). Просечно укупно преживљавање у подгрупи са високим нивоом прекомерне експресије ХЕР2 било је 11,8 месеци у односу на 16 месеци, ХР 0,65 (95% ЦИ 0,51-0,83) и преживљавање без прогресије било је 5,5 месеци у односу на 7,6 месеци, ХР 0,64 (95% ЦИ 0,51-0,79) у групи ФП у односу на групу ФП + Х, респективно. укупно преживљавање је било 0,75 (95% ЦИ 0,51-1,11) у ИХЦ2 + / ФИСХ + и 0,58 (95% ЦИ 0,41-0,81) у ИХЦ3 + / ФИСХ + групи.
У експлоративној анализи подгрупа извршеној у ТоГА студији (БО18255), није било очигледне укупне користи од преживљавања додавањем Херцептина код пацијената са основним ЕЦОГ ПС 2 [ХР 0,96 (95% ЦИ 0, 51-1,79)], немерљиво [ ХР 1,78 (95% ЦИ 0,87-3,66)] и локално узнапредовале [ХР 1,20 (95% ЦИ 0,29-4,97)] болести.
Педијатријска популација
Европска агенција за лекове укинула је обавезу да достави резултате студија са Херцептином у свим подгрупама у педијатријској популацији за рак желуца и дојке (видети одељак 4.2 за информације о педијатријској употреби).
05.2 Фармакокинетичка својства
Фармакокинетика трастузумаба процијењена је популационом фармакокинетичком анализом модела користећи збирне податке од 1582 испитаника са ХЕР2-позитивном МБЦ, ЕБЦ или узнапредовалим раком желуца (АГЦ), или другим раком., И здравих добровољаца, у 18 студија И, ИИ и ИИИ студије у коме је примењен Херцептин ИВ. За опис концентрације / временског профила коришћен је модел са два одељења са паралелном линеарном и нелинеарном елиминацијом из централног одељка. Због нелинеарне елиминације укупни клиренс се повећавао са смањењем концентрације. Стога, не може се закључити да постоји константна вредност времена полувремена трастузумаба .. т1 / 2 опада са смањењем концентрација у распону доза (видети Табелу 16.) Пацијенти са МБЦ и ЕБЦ имали су сличне вредности фармакокинетичких параметара [нпр. клиренс (ЦЛ), запремина одељка на централну (Вц) и популацију предвиђену стабилну изложеност (Цмин, Цмак и АУЦ)]. Линеарни клиренс је био 0,136 Л / дан за МБЦ, 0,112 Л / дан за ЕБЦ и 0,176 Л / дан за АГЦ. Вредности параметара нелинеарне елиминације биле су 8,81 мг / дан за максималну брзину елиминације (Вмак) и 8,92 мцг / мЛ за Мицхаелис-Ментенову константу (Км) за пацијенте са МБЦ, ЕБЦ и АГЦ. Запремина централног одељка била је 2,62 л за пацијенте са МБЦ и ЕБЦ и 3,63 л за пацијенте са АГЦ. коначни популацијски фармакокинетички модел идентификовао је телесну тежину, серумску аспартат аминотрансферазу и албумин као статистички коваријантне значајне ефекте који утичу на изложеност трастузумабу. Међутим, величина ефекта ових коваријата на изложеност трастузумабу сугерише мало вероватан клинички значајан утицај на концентрације трастузумаба.
Вредности изложености предвиђене популационом фармакокинетиком (медијана са 5. до 95. перцентилом) и вредност фармакокинетичких параметара у клинички значајним концентрацијама (Цмак и Цмин) за пацијенте са МБЦ, ЕБЦ и АГЦ лечене одобреним режимима дозирања к1в (недељно дозирање) и к3в (дозирање сваке три недеље) приказани су у Табели 14 (Циклус 1), Табели 15 (равнотежно стање) и Табели 16 (фармакокинетички параметри).
Табела 14 Фармакокинетичке вредности за популацију предвиђене изложености у циклусу 1 (медијан 5 - 95. перцентил) за режиме лечења Херцептином ИВ код пацијената са МБЦ, ЕБЦ и АГЦ
Табела 15 Вредности фармакокинетичке изложености у стању стабилног стања (од 5. до 95. перцентила) за популацију предвиђене у режиму стабилног стања за режиме лечења Херцептином ИВ код пацијената са МБЦ, ЕБЦ и АГЦ
* Цмин, сс - Цмин у стању мировања
** Цмак, сс = Цмак у стационарном стању
*** време на 90% равнотежног стања
Табела 16 Вредности фармакокинетичких параметара предвиђених за популацију у стабилном стању за ИВ режиме примене Херцептина код пацијената са МБЦ, ЕБЦ и АГЦ
Испирање трастузумабом
Период испирања трастузумаба је процењен након интравенске примене к1в или к3в применом популационог фармакокинетичког модела. Резултати ових симулација указују на то да ће најмање 95% пацијената постићи концентрацију
Циркулирајући растворљиви антиген
Истраживачке анализе коваријата са подацима за само једну подгрупу пацијената сугеришу да су субјекти са вишим нивоима ХЕР2-ЕЦД растворљивог антигена (СХЕД) имали бржи (нижи Км) нелинеарни клиренс (п СГОТ / АСТ; утицај растворљивог антигена на клиренс се приписује СГОТ / АСТ нивои.
Нема података о нивоу циркулишућег ванћелијског домена рецептора ХЕР2 (растворљиви антиген) у серуму пацијената са раком желуца.
05.3 Предклинички подаци о безбедности
Није било доказа о токсичности појединачне или поновљене дозе у студијама које су трајале до 6 месеци, нити о репродуктивној токсичности у студијама о тератологији, плодности или токсичности жена у последњем периоду гестације / плацентног пасажа. Херцептин није генотоксичан.А Студија трехалозе, једног од главних помоћних састојака формулације, није открила никакву токсичност.
Дуготрајна истраживања на животињама нису спроведена да би се утврдио канцерогени потенцијал Херцептина, нити да би се утврдили његови ефекти на плодност мушкараца.
06.0 ФАРМАЦЕУТСКЕ ИНФОРМАЦИЈЕ
06.1 Помоћне супстанце
Л-хистидин хидрохлорид
Л-хистидин
а, а-трехалоза дихидрат
полисорбат 20
06.2 Некомпатибилност
Овај медицински производ се не сме мешати или разблаживати са другим лековима осим оних који су поменути у одељку 6.6.
Не разблажујте растворима глукозе јер они изазивају накупљање протеина.
06.3 Период важења
4 године
Након реконституисања са водом за ињекције, реконституисани раствор остаје физички и хемијски стабилан 48 сати на 2 ° Ц до 8 ° Ц. Остаци реконституисаног раствора морају се одбацити.
Раствори Херцептина за инфузију у врећама од поливинилхлорида, полиетилена или полипропилена који садрже 9 мг / мЛ (0,9%) раствора натријум хлорида за ињекције остају физички и хемијски стабилни 24 сата на температурама које не прелазе 30 ° Ц.
Са микробиолошког становишта, реконституисани раствор и раствор за инфузију Херцептина треба одмах користити. Производ се не сме складиштити након реконституисања и разблаживања, осим ако је то учињено у контролисаним и валидираним асептичним условима. Ако се производ не користи одмах, време и услови складиштења у употреби су одговорност корисника.
06.4 Посебне мере предострожности при складиштењу
Чувати у фрижидеру (2 ° Ц - 8 ° Ц)
За услове складиштења након првог отварања, видети одељке 6.3 и 6.6.
06.5 Природа непосредног паковања и садржај паковања
Херцептин бочица:
Једна бочица од прозирног стакла од 15 мл типа И са затварачем од бутил гуме са ламинираним флуором садржи 150 мг трастузумаба.
Свако паковање садржи једну бочицу.
06.6 Упутства за употребу и руковање
Придржавајте се одговарајућих асептичних техника. Свака бочица Херцептина се реконституише са 7,2 мл стерилне воде за ињекције (не испоручује се). Избегавајте употребу других растварача за реконституисање. Ово даје 7,4 мЛ раствора за једну дозу, који садржи приближно 21 мг / мЛ трастузумаба, са пХ од приближно 6.0. Вишак запремине од 4% гарантује аспирацију из бочице програмираног доза од 150 мг.
Херцептином се мора пажљиво руковати током поступка реконституције. Прекомерно стварање пене услед реконституисања или мућкања реконституисаног раствора може изазвати проблеме са количином Херцептина која се може извући из бочице.
Реконституисани раствор се не сме замрзавати.
Упутства за реконституцију:
1) Стерилним шприцем полако убризгајте 7,2 мл воде за ињекције у бочицу која садржи лиофилизовани Херцептин, усмеравајући млаз према лиофилизованој супстанци.
2) Полако завртите бочицу како бисте олакшали реконституцију. НЕ ТРЕШАЈТЕ!
Благо стварање пене током реконституције није неуобичајено. Оставите бочицу да стоји усправно око 5 минута. Након реконституције, Херцептин претпоставља изглед бистрог, безбојног до свијетложутог раствора без видљивих честица.
Одредите потребну запремину раствора:
• на основу почетне дозе од 4 мг трастузумаба / кг телесне тежине, или накнадне недељне дозе од 2 мг трастузумаба / кг телесне тежине:
• на основу почетне дозе од 8 мг трастузумаба / кг телесне тежине, или накнадне дозе од 6 мг трастузумаба / кг телесне тежине сваке 3 недеље:
Извуците потребну количину раствора из бочице и додајте је у врећицу за инфузију која садржи 250 мл 0,9% раствора натријум хлорида. Немојте користити растворе који садрже глукозу (видети одељак 6.2). Врећицу треба пажљиво окренути да се раствор помеша како би се избегло стварање пене. Након што се припреми, инфузију треба одмах применити. Ако се разблажи према асептичним методама, може се чувати 24 сата (чувати на температури испод 30 ° Ц).
Раствори за парентералну примену треба да се пре примене визуелно прегледају на било какве честице или промену боје.
Херцептин је само за једнократну употребу, јер производ не садржи конзервансе. Неискоришћени лек и отпад добијени из овог лека морају се одложити у складу са локалним прописима.
Нису примећене некомпатибилности између врећица Херцептин и поливинилхлорида, полиетилена или полипропилена.
07.0 НОСИЛАЦ ОВЛАШЋЕЊА ЗА ПРОМЕТ
Роцхе Регистратион Лимитед
6 Фалцон Ваи
Схире Парк
Велвин Гарден Цити
АЛ7 1ТВ
УК
08.0 БРОЈ ОДЛИКЕ ЗА ПРОМЕТ
ЕУ/1/00/145/001
034949014
09.0 ДАТУМ ПРВОГ ОДОБРЕЊА ИЛИ ОБНОВЕ ОВЛАШЋЕЊА
Датум прве ауторизације: 28. август 2000
Датум последњег обнављања: 28. август 2010
10.0 ДАТУМ РЕВИЗИЈЕ ТЕКСТА
Септембра 2015